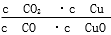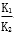题目内容
4.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )| A. | Na2CO3俗称纯碱,属于盐类,可用于洗涤油污等 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
分析 A.碳酸钠为强碱弱酸盐,水解显碱性;
B.锌的活泼性强于铁,二者形成原电池锌做负极;
C.耐高温材料应具有较高的熔点;
D.电解氯化镁溶液生成氢气、氯气、氢氧化镁沉淀.
解答 解:A.碳酸钠为强碱弱酸盐,俗称纯碱,水解显碱性,油污成分为油脂,油脂在碱性环境下水解生成可溶性物质,所以可以洗涤油污等,故A正确;
B.在海轮外壳上镶入锌块,锌的活泼性强于铁,二者形成原电池锌做负极,先发生氧化还原反应,可减缓船体的腐蚀速率,故B正确;
C.氧化镁熔点高,可以用来制造耐高温材料,故C正确;
D..电解氯化镁溶液生成氢气、氯气、氢氧化镁沉淀,得不到镁,电解熔融的氯化镁能够生成镁,故D错误;
故选:D.
点评 本题考查了元素化合物知识,熟悉相关物质的性质,明确金属电化学腐蚀原理,电解池工作原理是解题关键,题目难度不大.

练习册系列答案
相关题目
14.对下列实验操作和现象所作出的实验结论正确的是( )
| 实验操作和现象 | 实验结论 | |
| A | SO2通入Ba(NO3)2溶液中有白色沉淀生成 | 白色沉淀是BaSO3 |
| B | 向某待检液中滴加盐酸酸化的BaCl2溶液,生成白色沉淀 | 该待检液中可能不含有SO42- |
| C | 将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别滴加CCl4,振荡,静置,下层分别呈无色和紫红色 | 氧化性:Fe3+>Br2>I2 |
| D | 向浓度均为0.1mol/L的KCl、KI混合液中滴加1~2滴0.01mol/LAgNO3溶液,产生黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 某澄清透明溶液中:K+、Cu2+、NO3-、Cl- | |
| B. | 含0.1mol•L-1 Fe3+的溶液中:Na+、Mg2+、SO42-、Cl-、SCN- | |
| C. | 含0.1mol•L-1 CO32-的溶液中:OH-、Cl-、NH4+、Na+、H+ | |
| D. | 加入铝粉产生H2的溶液中:Al3+、Na+、SO42-、NO3- |
9.下列试剂可用带磨口玻璃塞的玻璃试剂瓶保存的是( )
| A. | 氢氟酸 | B. | 硫酸 | C. | 碳酸钠溶液 | D. | 氧氧化钠溶液 |
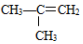 ②
②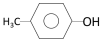 ;③
;③ ;④CH3CH2Cl;⑤CCl4;⑥CH3C≡CH;⑦HOCH2CH2OH;⑧CH3CH2OH;根据官能团的不同可分为( )
;④CH3CH2Cl;⑤CCl4;⑥CH3C≡CH;⑦HOCH2CH2OH;⑧CH3CH2OH;根据官能团的不同可分为( ) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)