题目内容
14.已知一些燃料的燃烧热的数据如表所示:| 燃料 | 一氧化碳 | 甲烷 | 正戊烷 | 乙醇 |
| △H/(kJ•mol-1) | -283.0 | -891.0 | -3761 | -1366.8 |
| A. | 一氧化碳 | B. | 甲烷 | C. | 正戊烷 | D. | 乙醇 |
分析 △H是焓变,其值为负值时,反应放热,负号后面的数字越大,放出的热量就越大;负号后面的数字越小,放出的热量就越小,一氧化碳、甲烷、正戊烷、乙醇的相对分子质量分别为28、16、72、46,所以相同质量的这4种燃料的物质的量之比就是:$\frac{1}{28}$:$\frac{1}{16}$:$\frac{1}{72}$:$\frac{1}{46}$,由此分析解答.
解答 解:△H是焓变,其值为负值时,反应放热,负号后面的数字越大,放出的热量就越大;负号后面的数字越小,放出的热量就越小,一氧化碳、甲烷、正戊烷、乙醇的相对分子质量分别为28、16、72、46,所以相同质量的这4种燃料的物质的量之比就是:$\frac{1}{28}$:$\frac{1}{16}$:$\frac{1}{72}$:$\frac{1}{46}$,燃烧放出热量分别为:283.0kJ×$\frac{1}{28}$=10.1kJ、891kJ×$\frac{1}{16}$=55.69KJ、3761kJ×$\frac{1}{72}$=52.2KJ、1366.8kJ×$\frac{1}{46}$=29.7kJ,所以相同质量的一氧化碳、甲烷、正戊烷、乙醇完全燃烧时,放出热量最多的是甲烷.
故选:B.
点评 此题是一道物质的质量及物质的量的转化题,解题的关键是能对相关的基本计算的掌握,属于一道基础性计算考查题.

练习册系列答案
相关题目
5.在2A+B═3C+4D反应中,表示该反应速率最快的数据是( )
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.8 mol•L-1•s-1 | D. | v(D)=1.0 mol•L-1•s-1 |
2.下列实验能达到测量要求的是( )
| A. | 用托盘天平称取35.20g NaCl固体 | |
| B. | 用25mL酸式滴定管量取15.80mL盐酸溶液 | |
| C. | 用10mL量筒量取8.50mL盐酸 | |
| D. | 用广泛pH试纸测得某溶液pH值为4.2 |
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 某澄清透明溶液中:K+、Cu2+、NO3-、Cl- | |
| B. | 含0.1mol•L-1 Fe3+的溶液中:Na+、Mg2+、SO42-、Cl-、SCN- | |
| C. | 含0.1mol•L-1 CO32-的溶液中:OH-、Cl-、NH4+、Na+、H+ | |
| D. | 加入铝粉产生H2的溶液中:Al3+、Na+、SO42-、NO3- |
6.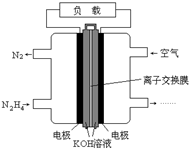 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )| A. | 电子从右侧电极经过负载后流向左侧电极 | |
| B. | 负极发生的电极反应式为:N2H4-4e-=N2+4H+ | |
| C. | 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 | |
| D. | 该燃料电池持续放电时.K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜 |
3.下列各组离子能够在指定环境下大量共存的是( )
| A. | 在pH=0的溶液中:Na+、K+、MnO4-、Cl- | |
| B. | 和Al反应能产生H2的溶液:K+、NH4+、Cl-、S2O32- | |
| C. | 中性溶液:Al3+、K+、SO42-、AlO2- | |
| D. | c(H+)<c(OH-)的溶液:Na+、K+、SO32-、S2- |