题目内容
16.下列说法正确的是( )| A. | C-O键的极性比N-O键的极性大 | |
| B. | CO和N2互为等电子体,且N2的沸点比CO的高 | |
| C. | H2CO3、H2SiO3、H3PO4酸性越来越弱 | |
| D. | 金属K采用面心立方堆积,空间利用率为74% |
分析 A.二者非金属性差距越大极性越大;
B.原子总数相同、价电子总数也相同的微粒互为等电子体,相对分子质量相同的,分子的极性越强分子间作用力越强熔沸点越高;
C.元素非金属性越强,最高价氧化物水化物的酸性越强;
D.金属K属于体心立方堆积.
解答 解:A.二者非金属性差距越大极性越大,所以C-O键的极性比N-O键的极性大,故A正确;
B.N2分子与CO分子中原子总数相同、价电子总数也相同,二者互为等电子体,CO和N2分子量相同,但是CO是极性分子,N2是非极性分子,所以熔沸点前者大于后者,故B错误;
C.元素非金属性越强,最高价氧化物水化物的酸性越强,非金属性:N>P>Si,酸性H3PO4>H2CO3>H2SiO3,故C错误;
D.金属K采用体心立方堆积,空间利用率为68%,故D错误;
故选A.
点评 本题考查键的极性、等电子体、沸点大小比较、非金属性的递变规律、金属K空间利用率等知识,D选项注意掌握典型晶体晶胞结构,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
6.将1.5mL0.1mol•L-1Na2SO4溶液和1.0mL0.1mol•L-1BaCl2溶液混合后得到浊液a,过滤得到滤液b和白色沉淀c.下列分析不正确的是( )
| A. | 浊液a中存在沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq) | |
| B. | 若向滤液b中滴加0.01mol•L-1Na2SO4溶液,无明显现象 | |
| C. | 若向滤液b中滴加0.01mol•L-1BaCl2溶液,会出现白色沉淀 | |
| D. | 若向滤液b中滴加0.01mol•L-1AgNO3溶液,无明显现象 |
7.下列贮存化学试剂的方法正确的是( )
| A. | 新制的氯水保存在棕色广口瓶中,并放在阴凉处 | |
| B. | 溴水存放在带玻璃塞的无色试剂瓶中 | |
| C. | 烧碱溶液放在带玻璃塞的磨口试剂瓶中 | |
| D. | 金属钠保存在煤油中 |
4.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn+MnO2+H2O=ZnO+Mn(OH)2,下列说法中,错误的是( )
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:MnO2+2H2O+2e-=Mn(OH)2+2OH- | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过0.2 mol电子,锌的质量理论上减少6.5 g |
1.反应4NH3(g)+5O2(g)$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O在2L的密闭容器中进行,30s后NO的物质的量增加了0.30mol.下列说法正确的是( )
| A. | 容器中NH3的物质的量一定增加了0.30mol | |
| B. | 容器中H2O(g)的物质的量至少为0.45mol | |
| C. | NH3的平均反应速率为0.010mol/(L•s) | |
| D. | NH3、O2、NO、H2O的物质的量之比一定为4:5:4:6 |
8.在2A(g)+B(g)=3C(g)+4D(g)中,表示该反应速率最快的是( )
| A. | v(A)=0.5mol•L-1•mim-1 | B. | v(B)=0.3mol•L-1•mim-1 | ||
| C. | v(C)=0.8mol•L-1•mim-1 | D. | v(D)=0.1mol•L-1•s-1 |
5.下列有机物名称正确的是( )
①2-乙基戊烷?②1,2-二氯丁烷?③2,2-二甲基-4-己醇 ④3,4-二甲基戊烷 ⑤二溴乙烷 ⑥1-甲基丙醇
⑦2-甲基-3-戊炔 ⑧2-甲基-1,3-丁二烯.
①2-乙基戊烷?②1,2-二氯丁烷?③2,2-二甲基-4-己醇 ④3,4-二甲基戊烷 ⑤二溴乙烷 ⑥1-甲基丙醇
⑦2-甲基-3-戊炔 ⑧2-甲基-1,3-丁二烯.
| A. | ①⑤⑥ | B. | ②③④ | C. | ②⑧ | D. | ③⑥⑦ |
6.根据下列物质变化,所得能量变化关系正确的是( )
| 物质变化 | 能量关系 | |
| A | 将充满NO2的针筒置于热水中,气体颜色变深 | 1molN2O4(g)的能量>2molNO2(g)的能量 |
| B | 将NaOH溶液与HCl溶液混合 | 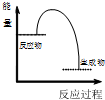 |
| C | 1g气态SiH4在空气中燃烧,生成SiO2 (s)与液态水,放热44.6kJ | SiH4(g)+2O2(g)→SiO2(s)+2H2O(l)+44.6kJ |
| D | 合成氨:N2(g)+3H2(g)?2NH3(g)+92.4kJ | 反应物的总键能>生成物的总键能 |
| A. | A | B. | B | C. | C | D. | D |
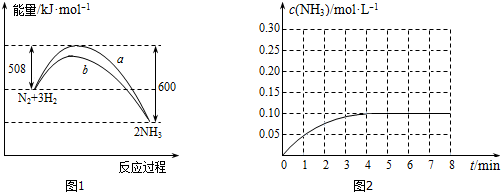
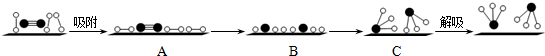
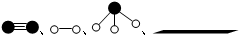 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用如图表示.吸附后,能量状态最高的是B (填字母序号).
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用如图表示.吸附后,能量状态最高的是B (填字母序号).