题目内容
下列现象与电化学腐蚀无关的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、生铁比软铁心(几乎是纯铁)容易生锈 |
| C、铁制器件附有铜质配件,在接触处易生锈 |
| D、铁丝在纯氧气中燃烧 |
考点:金属的电化学腐蚀与防护
专题:
分析:根据是否能构成原电池,如果能构成原电池就产生电化学腐蚀,否则不能产生电化学腐蚀,据此分析解答.
解答:
解:A、黄铜(铜锌合金)制作的铜锣中,金属锌为负极,金属铜做正极,Cu被保护,不易腐蚀,和电化学腐蚀有关,故A错误;
B、生铁中金属铁、碳、潮湿的空气能构成原电池,金属铁为负极,易被腐蚀而生锈,和电化学腐蚀有关,故B错误;
C、铁制器件附有铜质配件,在接触处金属铁和金属铜构成原电池中,金属铁是负极,易生锈,和电化学腐蚀有关,故C错误;
D、铁丝在纯氧气中燃烧生成四氧化三铁,是金属铁的化学性质的表现,和电化学腐蚀无关,故D正确;
故选D.
B、生铁中金属铁、碳、潮湿的空气能构成原电池,金属铁为负极,易被腐蚀而生锈,和电化学腐蚀有关,故B错误;
C、铁制器件附有铜质配件,在接触处金属铁和金属铜构成原电池中,金属铁是负极,易生锈,和电化学腐蚀有关,故C错误;
D、铁丝在纯氧气中燃烧生成四氧化三铁,是金属铁的化学性质的表现,和电化学腐蚀无关,故D正确;
故选D.
点评:本题以电化学腐蚀为载体考查了金属的腐蚀和防护,根据能否构成原电池来判断是否为电化学腐蚀即可,难度不大.

练习册系列答案
相关题目
 对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),NH3和H2的物质的量(n)随时间变化关系如图所示,下列叙述正确的是( )
对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),NH3和H2的物质的量(n)随时间变化关系如图所示,下列叙述正确的是( )| A、点e的正反应速率比点d大 |
| B、点c处v(逆)>v(正) |
| C、点d(t1时刻)和点e(t2时刻)处N2物质的量相同 |
| D、图中字母标记的五点中a点对应的NH3的物质的量最大 |
有机物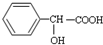 有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )
 有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中符合属于酯类且能与氯化铁溶液发生显色反应的同分异构体有多少种(不考虑立体异构)( )| A、6 种 |
| B、9 种 |
| C、15 种 |
| D、19 种 |
 控制适合的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池(盐桥起到导电作用).下列判断不正确的是( )
控制适合的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池(盐桥起到导电作用).下列判断不正确的是( )| A、反应开始时,乙中石墨电极上发生氧化反应 |
| B、反应开始时,甲中石墨电极作负极 |
| C、电流计读数为零时,反应达到化学平衡状态 |
| D、电流计读数为零后,在甲中溶入FeCl2,电流表可能会再次产生偏转 |
分析离子反应 xR2++yH++O2═mR3++nH2O,下列说法中正确的是( )
| A、n=2,H2O是氧化产物 |
| B、x=y=m=4 |
| C、该反应中R2+得到电子,被氧化为R3+ |
| D、任何氧化还原反应中氧化剂失电子总数都等于还原剂得电子总数 |
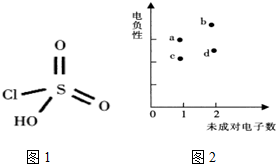 纯钛烤瓷牙是近几年才发展成熟的金属烤瓷技术,过氧硫酸被用于假牙的消毒.过氧硫酸可由氯磺酸通过反应I制得,氯磺酸结构如图1.
纯钛烤瓷牙是近几年才发展成熟的金属烤瓷技术,过氧硫酸被用于假牙的消毒.过氧硫酸可由氯磺酸通过反应I制得,氯磺酸结构如图1. (1)已知在一定条件下的反应4HCl+O2=2Cl2+2H2O中,有4mol HCl被氧化时,放出
(1)已知在一定条件下的反应4HCl+O2=2Cl2+2H2O中,有4mol HCl被氧化时,放出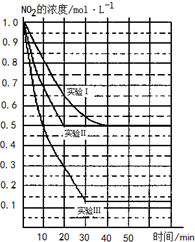 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题:
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题: