题目内容
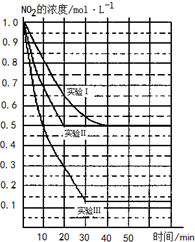 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题:
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题:(1)实验Ⅱ隐含的反应条件是
(2)写出该反应的平衡常数表达式:K=
(3)若实验Ⅰ中达平衡后,再向该密闭容器中通入1mol NO2与1mol NO混合气体(保持温度和体积不变),则平衡将
(4)一定条件下NO2与SO2可发生反应,其方程式为:NO2(g)+SO2(g)?SO3(g)+NO(g)△H>0,将NO2与SO2以体积比1:2置于体积固定的密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A、混合气体的压强保持不变
B、混合气体的颜色保持不变
C、SO3和NO的体积比保持不变
D、混合气体的平均相对分子质量保持不变
E、混合气体的密度保持不变
F、混合气体对于氢气的相对密度保持不变
(5)对于(4)中的反应,若改变条件,使平衡常数变大,则该反应
A、一定向正反应方向移动
B、在平衡移动时,正反应速率先增大后减小
C、一定向逆反应方向移动
D、在平衡移动时,逆反应速率先增大后减小.
考点:物质的量或浓度随时间的变化曲线,化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:(1)实验Ⅰ和实验Ⅱ平衡时NO2的浓度相同,但实验Ⅱ反应速率大;
(2)化学平衡常数为生成物浓度系数次幂之积与反应物浓度系数次幂之积的比值;
(3)根据平衡常数和浓度商判断平衡移动;
(4)根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡;
(5)化学平衡常数只与温度有关,由于该反应为吸热反应,升温,平衡右移,K增大,v(正)、v(逆)均增大.
(2)化学平衡常数为生成物浓度系数次幂之积与反应物浓度系数次幂之积的比值;
(3)根据平衡常数和浓度商判断平衡移动;
(4)根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡;
(5)化学平衡常数只与温度有关,由于该反应为吸热反应,升温,平衡右移,K增大,v(正)、v(逆)均增大.
解答:
解:(1)实验Ⅱ和实验Ⅰ比较,达到平衡所用时间短,但平衡不移动,所以实验Ⅱ隐含条件为使用了催化剂,故答案为:使用了催化剂;
(2)化学平衡常数为生成物浓度系数次幂之积与反应物浓度系数次幂之积的比值,故答案为:
;
(3)实验Ⅰ中,平衡时c(NO2)=0.5mol?L-1,c(NO)=0.5mol?L-1,c(O2)=0.25mol?L-1,
即 2NO2(g)?2NO(g)+O2(g)
0.5mol?L-1 0.5mol?L-1 0.25mol?L-1
K=
=0.25.当再加入0.25mol?L-1NO2、0.25mol?L-1NO时,Qc=
=0.25,所以平衡不移动,故答案为:不移动;
(4)A.反应NO2(g)+SO2(g)?SO3(g)+NO(g)是反应前后气体分子数不变的反应,故体系的压强保持不变,不能说明反应已经处于平衡状态,故A错误;
B.随着反应的进行,NO2的浓度减小,颜色变浅,当颜色保持不变时说明反应处于平衡状态,故B正确;
C.SO3和NO都是生成物,比例始终保持1:1,所以当SO3和NO的体积比保持不变时,无法判断反应是否处于平衡状态,故C错误;
D.M=
,反应前后气体质量不变,反应前后气体体积不变,相对分子质量不随化学平衡移动而变化,不能判断是否达到化学平衡状态,故D错误;
E.由于反应在固定容积中进行,反应前后气体的质量始终不变,所以反应过程中密度也不变,所以混合气体的密度保持不变不能判断反应是否处于平衡状态,故E错误;
F.由于混合气体在反应过程中密度始终保持不变,所以对氢气的相对密度也保持不变,所以当混合气体对于氢气的相对密度保持不变时,不能判断反应是否处于平衡状态,故F错误;
故选B;
(5))化学平衡常数只与温度有关,△H>0,该反应为吸热反应,升温,平衡右移,K增大,v(正)、v(逆)均增大,A、B正确,故答案为:AB.
(2)化学平衡常数为生成物浓度系数次幂之积与反应物浓度系数次幂之积的比值,故答案为:
| c2(NO)?c(O2) |
| c2(NO2) |
(3)实验Ⅰ中,平衡时c(NO2)=0.5mol?L-1,c(NO)=0.5mol?L-1,c(O2)=0.25mol?L-1,
即 2NO2(g)?2NO(g)+O2(g)
0.5mol?L-1 0.5mol?L-1 0.25mol?L-1
K=
| 0.52×0.25 |
| 0.52 |
| (0.5+0.5)2×0.25 |
| (0.5+0.5)2 |
(4)A.反应NO2(g)+SO2(g)?SO3(g)+NO(g)是反应前后气体分子数不变的反应,故体系的压强保持不变,不能说明反应已经处于平衡状态,故A错误;
B.随着反应的进行,NO2的浓度减小,颜色变浅,当颜色保持不变时说明反应处于平衡状态,故B正确;
C.SO3和NO都是生成物,比例始终保持1:1,所以当SO3和NO的体积比保持不变时,无法判断反应是否处于平衡状态,故C错误;
D.M=
| m |
| n |
E.由于反应在固定容积中进行,反应前后气体的质量始终不变,所以反应过程中密度也不变,所以混合气体的密度保持不变不能判断反应是否处于平衡状态,故E错误;
F.由于混合气体在反应过程中密度始终保持不变,所以对氢气的相对密度也保持不变,所以当混合气体对于氢气的相对密度保持不变时,不能判断反应是否处于平衡状态,故F错误;
故选B;
(5))化学平衡常数只与温度有关,△H>0,该反应为吸热反应,升温,平衡右移,K增大,v(正)、v(逆)均增大,A、B正确,故答案为:AB.
点评:本题考查图象与化学平衡,明确影响化学平衡的因素及图象中量的是解答本题的关键,(3)是学生解答中的难点,注意利用K与Q来分析平衡移动的方法.

练习册系列答案
相关题目
下列现象与电化学腐蚀无关的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、生铁比软铁心(几乎是纯铁)容易生锈 |
| C、铁制器件附有铜质配件,在接触处易生锈 |
| D、铁丝在纯氧气中燃烧 |
2012年4月,卫生部在官网发布了拟撤销2,4-二氯苯氧乙酸等38种食品添加剂意见函,并公开征求意见.下列有关食品添加剂的说法正确的是( )
| A、需要长时间储存的食品应加入适宜的防腐剂 |
| B、冰激凌不使用着色剂营养价值一定会降低 |
| C、炒菜时拒绝添加食盐、味精等各种调味剂 |
| D、色、香、味俱全的食物营养价值不一定高 |
 Ⅰ、(将2mol SO2和1mol O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g) 2SO3 (g).若经过2s后测得SO3的浓度为0.6mol/L.试计算:(1)O2的化学反应速率V(O2)=
Ⅰ、(将2mol SO2和1mol O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g) 2SO3 (g).若经过2s后测得SO3的浓度为0.6mol/L.试计算:(1)O2的化学反应速率V(O2)=