题目内容
18.下列关于物质应用和组成的说法正确的是( )| A. | 浓硫酸可用于干燥Cl2和NH3 | |
| B. | 正常雨水的pH小于7 | |
| C. | CCl4可用于萃取碘水中的碘,但酒精不可以用于萃取碘水中的碘 | |
| D. | Si可用于制造光导纤维 |
分析 A.浓硫酸具有酸性和强氧化性,不能干燥碱性和还原性气体;
B.依据酸雨的定义解答;
C.萃取剂的选择必须符合下列条件:溶质在萃取剂中的溶解度比在原溶剂中要大;萃取剂与原溶剂不相溶;萃取剂与溶质不反应;
D.二氧化硅可以制造光导纤维.
解答 解:A.氨气为碱性气体,不能用浓硫酸干燥,故A错误;
B.酸雨是指PH<5.6的雨水,故B正确;
C.碘易溶于四氯化碳,且与水互不相溶,密度与水不同,而酒精与水混溶,所以CCl4可用于萃取碘水中的碘,但酒精不可以用于萃取碘水中的碘,故C正确;
D.用于制造光导纤维的为二氧化硅,不是硅,故D错误;
故选:BC.
点评 本题考查了物质的性质和用途,萃取实验,明确萃取剂选择原则,熟悉浓硫酸、二氧化硅的性质是解题关键,注意对酸雨概念的把握.

练习册系列答案
相关题目
8.为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
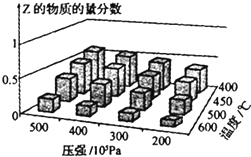

| A. | 在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平衡时,Z的物质的量分数增大 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H>0 m+n>c | |
| D. | 温度不变,减小压强,平衡逆向移动,达新平衡时,A的浓度比原平衡减小 |
9.常温常压下,既有颜色又有刺激性气味的气体是( )
| A. | CO | B. | SO2 | C. | Cl2 | D. | NH3 |
13.下列有关乙烯的说法不正确的是( )
| A. | 溴水中通入乙烯气体后,颜色会褪去 | |
| B. | 一定条件下,溴水可与氢气发生加成反应 | |
| C. | 乙烯可令酸性高锰酸钾溶液褪色 | |
| D. | 乙烯可燃,完全燃烧后产生CO2和水 |
3.下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
| A. | 1mol•L-1NaCl溶液含有NA个Na+ | |
| B. | 1 L 0.1mol•L-1氨水含有0.1NA个OH- | |
| C. | 电解饱和食盐水若产生2g氢气,则转移2NA个电子 | |
| D. | 将0.1mol氯化铁溶于1 L水中,所得溶液含有0.1NA个Fe3+ |
7.下列说法正确的是( )
| A. | 114号元素在周期表中第七周期第VIA族,属于金属元素 | |
| B. | 晶体硅熔点高硬度大,可用于制作光导纤维 | |
| C. | 光束通过下列分散系①有尘埃的空气②胆矾溶液③墨水④稀豆浆时,均产生丁达尔效应 | |
| D. | 为了除去MgCl2酸性溶液中的Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入MgCO3,过滤后,再向滤液中加入适量的盐酸 |
8.一定量的KMnO4固体与足量的100mL浓盐酸反应,其反应方程式为:2KMnO4+16HCl(浓)=2KCl+5Cl2↑+2MnCl2+8H2O,反应结束后,共转移电子2mol,则还原产物中,阳离子的物质的量浓度为(溶液的体积变化忽略不计)( )
| A. | 1mol/L | B. | 0.1mol/L | C. | 4mol/L | D. | 0.4mol/L |