题目内容
1.下列实验的解释或结论正确的是( )| 选项 | 实验 | 解释或结论 |
| A | 向包有Na2O2的脱脂棉滴少量水,脱脂棉燃烧 | Na2O2与H2O反应放热并有O2生成 |
| B | 向NaI溶液滴加FeCl3溶液,再加入CCl4,振荡,静置,下层呈紫红色 | 氧化性:I2>Fe3+ |
| C | 取酸雨试样,滴加H2O2溶液,再加入BaCl2溶液,有白色沉淀 | 该酸雨试样中一定含有H2SO3 |
| D | 用激光笔照射水玻璃(Na2SiO3的溶液),有丁达尔现象 | SiO32-水解生成了硅酸胶体 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.向包有Na2O2的脱脂棉滴少量水,脱脂棉燃烧,说明该反应为放热反应,且放出氧气;
B.下层呈紫红色,说明碘离子被铁离子氧化成碘单质,则氧化性I2<Fe3+;
C.酸雨中可能只含有硫酸,不一定含有亚硫酸;
D.丁达尔现象为胶体的性质,说明溶液中存在硅酸胶体.
解答 解:A.过氧化钠与水反应放出氧气,该反应为放热反应,导致脱脂棉燃烧,故A正确;
B.向NaI溶液滴加FeCl3溶液,再加入CCl4,振荡,静置,下层呈紫红色,说明碘离子被铁离子氧化,则氧化性:I2<Fe3+,故B错误;
C.取酸雨试样,滴加H2O2溶液,再加入BaCl2溶液,有白色沉淀,该白色沉淀为硫酸钡,但是原溶液中可能含有硫酸,不一定含有H2SO3,故C错误;
D.用激光笔照射水玻璃(Na2SiO3的溶液),有丁达尔现象,此为胶体的性质,说明SiO32-水解生成了硅酸胶体,故D正确;
故选AD.
点评 本题考查了化学实验方案的设计与评价,涉及过氧化钠性质、氧化性强弱比较、酸雨的成因、胶体的性质等知识,明确常见元素及其化合物性质为解答关键,试题培养了学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
12.关于氢键的下列说法中正确的是( )
| A. | 每个水分子内含有两个氢键 | |
| B. | 只要有氢元素就能形成氢键 | |
| C. | 分子间能形成氢键使物质的熔点和沸点升高 | |
| D. | HF的稳定性很强,是因为其分子间能形成氢键 |
9.下列说法正确的是( )
| A. | 含有食品添加剂的物质均对人体健康有害 | |
| B. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 | |
| C. | 现代海战通过喷放液体SiCl4(极易水解)和液氨可产生烟幕,其主要成分是NH4Cl | |
| D. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
16.25℃时,常见的无机酸在水溶液中的电离子平衡常数如表,下列选项正确的是( )
| 氢氰酸(HCN) | 碳酸(H2C03) | 氢氟酸(HF) |
| K=4.9×10-10 | K1=4.4×10-7 K2=4.7×10-11 | K=6.61×10-4 |
| A. | 氰化钠溶液中通入少量CO2:2CN-+H2O+CO2═2HCN+CO32- | |
| B. | NaCN与HCN的混合溶液中一定有:c(Na+)>c(CN-)>c(HCN)>c(H+)>c(OH+) | |
| C. | 0.2 mol•L-1 HCN溶液与0.1mol•L-1NaOH溶液等体积混合后,溶液中各种离子的浓度关系有:2[c(H+)-c(OH+)]=c(CN+)-c(HCN) | |
| D. | 等体积、等浓度的NaCN和NaF溶液中所含离子总数前者大于后者 |
6.关于下列物质的关系中不正确的是( )
| A. | 金刚石与石墨互为同素异形体 | B. | H、D、T互为同位素 | ||
| C. | CH3-CH3与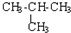 互为同系物 互为同系物 | D. | 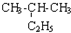 与 与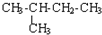 互为同分异构体 互为同分异构体 |
13.下列关于乙烯和乙烷的说法正确的是( )
| A. | 乙烷可与氯气反应制取纯净的一氯乙烷 | |
| B. | 乙烯可以使溴水褪色 | |
| C. | 乙烷和乙烯互为同分异构体 | |
| D. | 乙烯制备聚乙烯是物理变化 |
10.用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨).下列有关叙述不正确的是( )
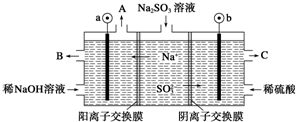

| A. | 图中a极连接电源的负极 | |
| B. | A口放出的物质是氢气,C口放出的物质是氧气 | |
| C. | b极电极反应式为:SO32--2e-+H2O═SO42-+2H+ | |
| D. | 电解过程中阴极区碱性明显增强 |
11.下列事实中,能说明B(OH)2是弱碱的是( )
| A. | 等体积的0.010mol/LB(OH)2溶液与0.010mol/LH2SO4溶液恰好完全反应 | |
| B. | 0.010mol/LB(OH)2溶液能使红色石蕊试液变蓝 | |
| C. | 0.010mol/LBCl2溶液呈酸性,0.010mol/LB2CO3溶液呈中性 | |
| D. | 0.010mol/LB(OH)2溶液能够与NH4Cl反应生成NH3(g) |
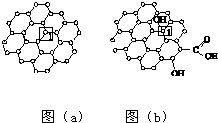 石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示].
石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示].