题目内容
2.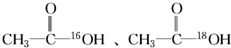 分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )
分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )| A. | 前者大于后者 | B. | 前者小于后者 | C. | 前者等于后者 | D. | 无法确定 |
分析 羧酸跟醇的反应过程是:羧酸分子中羧基中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯.
解答 解:羧酸跟醇的反应,羧酸分子中羧基中的羟基与醇分子中羟基的氢原子结合成水,
CH3CO16OH+H-O-C2H5 $?_{△}^{浓硫酸}$CH3COO-C2H5 +H216O;
CH3CO18OH+H-O-C2H5 $?_{△}^{浓硫酸}$CH3COO-C2H5 +H218O;
则两者生成酯的相对分子质量相等,
故选:C.
点评 本题考查酯化反应,难度较小,注意酯化反应原理是酸分子中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案
相关题目
12.下列说法正确的是( )
| A. | 氯化钾溶液在电流作用下电离成钾离子和氯离子 | |
| B. | 二氧化硫溶于水能部分转化成离子,故二氧化硫属于弱电解质 | |
| C. | 纯净的电解质在液态时,有的导电有的不导电 | |
| D. | 硫酸钡难溶于水,所以硫酸钡属弱电解质 |
13.图是某只含有C、H、O元素的有机物简易球棍模型,下列关于该有机物的说法正确的是( )
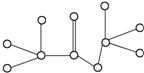

| A. | 分子式为C3H8O2 | |
| B. | 该物质属于酯类 | |
| C. | 该物质可由乙酸与乙醇反应制得 | |
| D. | 该物质含有双键,能跟氢气发生加成反应 |
10.对于反应:2H2S+SO2═3S+2H2O,被氧化的硫原子与被还原的硫原子的质量之比为( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 1:2 |
17.含n克HNO3的稀溶液恰好与m克Fe完全反应,若HNO3只被还原为NO,则n:m可能是 ①5:1、②9:2、③3:1、④2:1、⑤4:1( )
| A. | ②③⑤ | B. | ①③④ | C. | ②③④ | D. | ①③ |
7.有关如图所示化合物的说法不正确的是( )
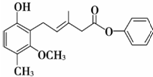

| A. | 该化合物既可以催化加氢,又可以在光照下与Cl2发生取代反应 | |
| B. | 该化合物既可以与溴水反应,又可以使酸性KMnO4溶液褪色 | |
| C. | 该化合物既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2 | |
| D. | 1 mol该化合物最多可以与3mol NaOH反应 |
14.下列说法不正确的是( )
| A. | 常见的周期表中,共有七个周期,三个短周期、四个长周期 | |
| B. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 | |
| C. | 短周期元素,是指一、二、三周期,分别有2、8、8种元素 | |
| D. | ⅠA中的金属元素,称为碱金属元素,ⅦA元素又称为卤族元素 |
12.下列含有非极性键的化合物是( )
| A. | MgCl2 | B. | Na2O2 | C. | H2O | D. | N2 |