题目内容
12.下列说法正确的是( )| A. | 氯化钾溶液在电流作用下电离成钾离子和氯离子 | |
| B. | 二氧化硫溶于水能部分转化成离子,故二氧化硫属于弱电解质 | |
| C. | 纯净的电解质在液态时,有的导电有的不导电 | |
| D. | 硫酸钡难溶于水,所以硫酸钡属弱电解质 |
分析 A、电离不需要电流的作用;
B、电解质导电必须是自身电离;
C、共价化合物在液态时,不导电,离子化合物在液态时导电;
D、强电解质指在水溶液中或熔融状态下能完全电离.
解答 解:A、氯化钾溶液在水分子作用下电离成钾离子和氯离子,故A错误;
B、二氧化硫溶于水生成亚硫酸,亚硫酸能部分电离成离子,而二氧化硫不能电离,故二氧化硫属于非电解质,故B错误;
C、纯净的强电解质在液态时,若为共价化合物在液态时不导电,若为离子化合物在液态时导电,故C正确;
D、强电解质指在水溶液中或熔融状态下,能完全电离,硫酸钡属于强电解质,虽在水溶液中很难溶解,但溶于水的部分能完全电离,故D错误;
故选C.
点评 本题主要考查了电解质、非电解质的概念以及导电条件,难度中等,注意知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
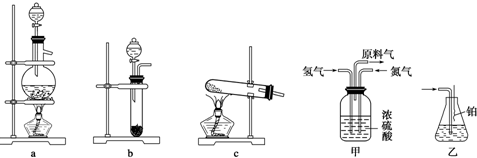
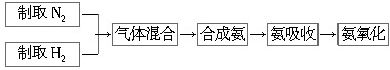
19. 工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
(1)已知:
N2(g)+O2(g)═2NO(g)△H=+a kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-b kJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-c kJ•mol-1
若有34g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为(1.5c-a-b)kJ.
(2)合成NH3达到平衡后,某时刻改变下列条件A,在达到新平衡的过程中正反应速率始终增大.
A.升温 B.加压 C.增大c(N2) D.降低c(NH3)
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如如图1所示:(图中T表示温度,n表示起始时H2物质的量)
①图象中T2和T1的关系是:T2<T1(填“>”、“<”、“=”或“无法确定”).
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是c(填字母).
③若容器容积为1L,b点对应的n=0.15mol,测得平衡时H2的转化率为60%,则平衡时N2的物质的量浓度为0.02 mol•L-1.
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同条件、不同时间段内合成NH3反应中N2的转化率,得到数据如表:
表中a、b、80%三者的大小关系为80%<a=b或80%<a<b.(填“>”、“=”、“<”、“无法比较”)
(5)向绝热、恒容的密闭容器中通入H2、N2使其在一定条件下合成NH3,请在图2中画出平衡常数K随时间的变化曲线.
 工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
工业上用N2和H2 合成NH3“N2(g)+3H2(g)═2NH3(g)△H<0”,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:(1)已知:
N2(g)+O2(g)═2NO(g)△H=+a kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-b kJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-c kJ•mol-1
若有34g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为(1.5c-a-b)kJ.
(2)合成NH3达到平衡后,某时刻改变下列条件A,在达到新平衡的过程中正反应速率始终增大.
A.升温 B.加压 C.增大c(N2) D.降低c(NH3)
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如如图1所示:(图中T表示温度,n表示起始时H2物质的量)
①图象中T2和T1的关系是:T2<T1(填“>”、“<”、“=”或“无法确定”).
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是c(填字母).
③若容器容积为1L,b点对应的n=0.15mol,测得平衡时H2的转化率为60%,则平衡时N2的物质的量浓度为0.02 mol•L-1.
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同条件、不同时间段内合成NH3反应中N2的转化率,得到数据如表:
 | 1小时 | 2 小时 | 3小时 | 4小时 |
| T3 | 30% | 50% | 80% | 80% |
| T4 | 35% | 60% | a | b |
(5)向绝热、恒容的密闭容器中通入H2、N2使其在一定条件下合成NH3,请在图2中画出平衡常数K随时间的变化曲线.
20.能证明乙酸是弱酸的实验事实是( )
| A. | CH3COOH溶液与Zn反应放出H2 | |
| B. | 0.1 mol/L CH3COONa溶液的pH大于7 | |
| C. | CH3COOH溶液与Na2CO3反应生成CO2 | |
| D. | 0.1 mol/L CH3COOH溶液可使紫色石蕊变红 |
17.下列物质不可能是烯烃加成产物的是( )
| A. | CH2ClCH3 | B. | CH3CH3 | C. | 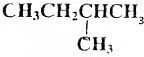 | D. | 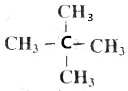 |
17.下列离子方程式书写正确的是( )
| A. | AgNO3溶液滴入少量的Na2S溶液 2Ag++S2-═Ag2S↓ | |
| B. | 向 溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- 溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| C. | 向Na2CO3溶液中加入过量CH3COOH溶液 CO32-+2H+═CO2↑+H2O | |
| D. | 向Ba(OH)2溶液中加入少量的NaHSO3溶液 2HSO3-+Ba2++2OH-═BaSO3↓+SO32-+2H2O |
2.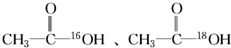 分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )
分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )
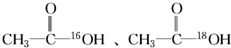 分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )
分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )| A. | 前者大于后者 | B. | 前者小于后者 | C. | 前者等于后者 | D. | 无法确定 |
 ;
; ;
;