题目内容
17.含n克HNO3的稀溶液恰好与m克Fe完全反应,若HNO3只被还原为NO,则n:m可能是 ①5:1、②9:2、③3:1、④2:1、⑤4:1( )| A. | ②③⑤ | B. | ①③④ | C. | ②③④ | D. | ①③ |
分析 Fe和稀硝酸反应方程式为3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O、Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,根据方程式计算被还原的硝酸的物质的量分析解答.
解答 解:含n克HNO3的稀溶液恰好与m克Fe完全反应,生成硝酸铁时,发生Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,溶解Fe的质量最小,根据电子转移守恒n(NO)=$\frac{mg}{56g/mol}$×$\frac{3}{5-2}$=$\frac{m}{56}$mol,
根据氮原子守恒可知n(HNO3)=n(NO)+3n[Fe(NO3)3],即$\frac{m}{56}$mol+$\frac{m}{56}$mol×3=$\frac{ng}{63g/mol}$,整理得整理得2n=9m,
生成硝酸亚铁时溶解Fe的质量最大,根据电子转移守恒n(NO)=$\frac{mg}{56g/mol}$×$\frac{2}{5-2}$=$\frac{m}{84}$mol,
根据氮原子守恒可知n(HNO3)=n(NO)+2n[Fe(NO3)2],
则$\frac{m}{84}$mol+2×$\frac{m}{56}$mol=$\frac{ng}{63g/mol}$,整理得n=3m
故m的取值范围为:$\frac{2}{9}$n≤m≤$\frac{1}{3}$n,②③⑤都符合,
故选A.
点评 本题考查了氧化还原反应的配平及计算,为高频考点,侧重于学生的分析能力和计算能力的考查,题目难度较大.注意利用极限法解答该题.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案
相关题目
5.区分晶体和非晶体最可靠的科学方法是( )
| A. | 观察外观是否规则 | B. | 测定是否有固定的熔点 | ||
| C. | 进行X射线衍射实验 | D. | 验证是否有各向异性 |
2.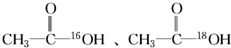 分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )
分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )
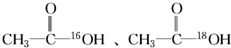 分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )
分别与CH3CH2OH反应,生成的酯的相对分子质量大小关系( )| A. | 前者大于后者 | B. | 前者小于后者 | C. | 前者等于后者 | D. | 无法确定 |
9.aLCO2气体通过足量Na2O2后所得气体再与bLNO混合时,可得到c L气体(气体体积均在相同状况下测定).下列表达式错误的是( )
| A. | 若a<b,则c<$\frac{1}{2}$(a+b) | B. | 若a<b,则c>$\frac{1}{2}$(a+b) | C. | 若a>b,则c=$\frac{1}{2}$(a+b) | D. | 若a=b,则c=$\frac{1}{2}$(a+b) |
6.A、B、C、D为原子序数依次增大的四种短周期元素,A原子的最外层上有4个电子;B和C能形成化合物C2B、C2B2,C单质的焰色反应呈现黄色;D的L层电子数等于K、M两个电子层上电子数之和.下列说法正确的是( )
| A. | 非金属性A>B>D | |
| B. | B和C形成的化合物中可能有共价键 | |
| C. | 原子序数D>C>A>B | |
| D. | 四种元素中,最高价氧化物对应的水化物酸性最强的是B |
7.以葡萄糖为燃料的微生物燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中,正确的是( )


| A. | 燃料电池的正极反应式为:O2+2H2O+4e-=4OH- | |
| B. | 装置中NaOH溶液的作用是吸收产生的有毒气体氯气 | |
| C. | 装置中的电子流动路径为:负极→外电路→阴极→苦卤水→阳极→正极 | |
| D. | 理论上,当b 极周围产生2g H2,电池消耗C6H12O6的质量为15g |
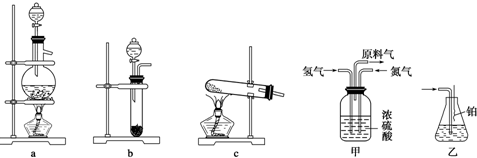
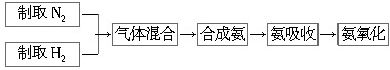

 .
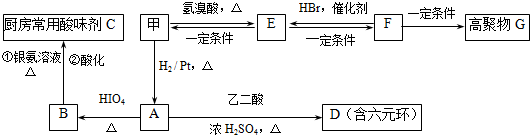
.
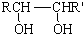 $→_{△}^{HIO_{4}}$ RCHO+R′CHO
$→_{△}^{HIO_{4}}$ RCHO+R′CHO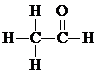 .
.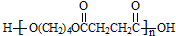 .
.