题目内容
18.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压下,8g甲烷中含C-H键的数目为4NA | |
| B. | 25℃时,1L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 1 mol冰醋酸和1mol乙醇经催化加热反应生成H2O的分子数为NA | |
| D. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA |
分析 A、求出甲烷的物质的量,然后根据甲烷中含4条C-H键分析;
B、pH=13的氢氧化钡溶液中氢氧根的浓度为0.1mol/L;
C、酯化反应为可逆反应;
D、求出氯气的物质的量,然后根据氯气和碱的反应为歧化反应来分析.
解答 解:A、8g甲烷的物质的量为0.5mol,而甲烷中含4条C-H键,故0.5mol甲烷中含2NA条C-H键,故B错误;
B、pH=13的氢氧化钡溶液中氢氧根的浓度为0.1mol/L,故1L溶液中含有的氢氧根的物质的量为0.1mol,故个数为0.1NA个,故B错误;
C、酯化反应为可逆反应,不能进行彻底,故生成的水分子个数小于NA个,故C错误;
D、标况下2.24L氯气的物质的量为0.1mol,而氯气和碱的反应为歧化反应,故0.1mol氯气转移0.1NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
11.下列各组溶液中,c(NO3-)与200mL0.2mol•L-1Na2SO4溶液中的c(SO42-)相同的是( )
| A. | l00mL0.4 mol•L-1KNO3溶液 | B. | 100mL0.2mol•L-1Cu(NO3)2溶液 | ||
| C. | 200mLO.l mol•L-1Fe(NO3)2溶液 | D. | 400mLO.l mol•L-1Al(NO3)3溶液 |
9.下列各有机物的名称错误的是( )
| A. | 3-甲基-2-戊烯 | B. | 3-甲基-2-丁烯 | C. | 2,2-二甲基丙烷 | D. | 3-甲基-1-丁炔 |
3. 图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )
图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )
 图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )
图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )| A. | 向NaAlO2溶液中逐渐滴入HCl至过量 | |
| B. | 向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量 | |
| C. | 向澄清石灰水中通入CO2至过量 | |
| D. | 向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量 |
10.下列有关阿伏伽德罗常数NA说法正确的是( )
| A. | 22 g 2H218O中含有的质子数为10NA | |
| B. | 标准状况下,2.24 L乙醇中含有的C-H键数目为0.5NA | |
| C. | 0.1 mol/L的NaF溶液中所含F-的数目小于0.1NA | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去0.5NA个电子 |

 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
.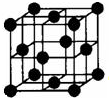 早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成.回答下列问题:
早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成.回答下列问题: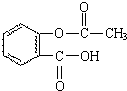 化学和环境保护、食品营养、材料应用等密切相关.
化学和环境保护、食品营养、材料应用等密切相关. .
.