��Ŀ����
14��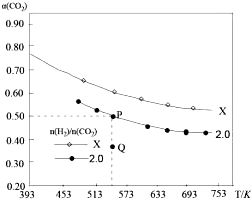 �������̶��ݻ���Ϊ1L�ܱ��������Բ�ͬ����̼��$\frac{n��{H}_{2}��}{n��C{O}_{2}��}$����H2��CO2����һ�������·�����Ӧ��2CO2��g��+6H2 ��g��?C2H4��g��+4H2O��g����H��CO2��ƽ��ת����a��CO2�����¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
�������̶��ݻ���Ϊ1L�ܱ��������Բ�ͬ����̼��$\frac{n��{H}_{2}��}{n��C{O}_{2}��}$����H2��CO2����һ�������·�����Ӧ��2CO2��g��+6H2 ��g��?C2H4��g��+4H2O��g����H��CO2��ƽ��ת����a��CO2�����¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �÷�Ӧ�ڸ������Է����� | |
| B�� | X����̼��X��2.0����Q������̼��Ϊ2.0ʱv��������v���棩 | |
| C�� | ����ʼʱ��CO2��H2Ũ�ȷֱ�Ϊ0.5mol/L��1.0mol/L����ɵõ�P�㣬��Ӧ�¶ȵ�ƽ�ⳣ����ֵΪ512 | |
| D�� | ����P��״̬�������У���2��4��1��4�ı����ٳ���CO2��H2��C2H4��H2O���ٴ�ƽ���a��CO2����С |
���� A����ͼ���֪�¶�����CO2��ת���ʽ��ͣ�˵��ƽ�������ƶ������H��0����ϡ�H-T•��S��0���Է������жϣ�
B������̼��Ϊ2.0ʱ��P���ƽ�⣬Q��δ��ƽ�⣬��ʱ������̼��ת���ʱ�ƽ��ʱС��˵����ʱҪ����ת������Ķ�����̼����Ӧ���������ƶ���
C������ʼʱ��CO2��H2Ũ�ȷֱ�Ϊ0.5mol/L��1.0mol/L����ʱ������̼��ת����Ϊ50%����������ʵ�ƽ��Ũ�ȣ��ɼ���ƽ�ⳣ����
D����2��4��1��4�ı����ٳ���CO2��H2��C2H4��H2O���൱���ٰ���4��10����CO2��H2����̼�ȴ���2��
��� �⣺A����ͼ���֪�¶�����CO2��ת���ʽ��ͣ�˵��ƽ�������ƶ������H��0���ɡ�S��0��֪��������¡�H-T•��S��0�������Է����У���A����
B������̼��Ϊ2.0ʱ��P���ƽ�⣬Q��δ��ƽ�⣬��ʱ������̼��ת���ʱ�ƽ��ʱС��˵����ʱҪ����ת������Ķ�����̼����Ӧ���������ƶ���������Ӧ���ʴ����淴Ӧ���ʣ���B����
C�� 2CO2��g��+6H2 ��g��?C2H4��g��+4H2O��g��
��ʼ 0.5 1 0 0
ת�� 0.25 0.75 0.125 0.5
ƽ�� 0.25 0.25 0.125 0.5
K=$\frac{0.125��0��{5}^{4}}{0.2{5}^{2}��0.2{5}^{6}}$=512����C��ȷ��
D����2��4��1��4�ı����ٳ���CO2��H2��C2H4��H2O���൱���ٰ���4��10����CO2��H2����̼�ȴ���2�����ƽ���a��CO2������D����
��ѡC��
���� ���⿼�黯ѧƽ�������Ӱ�����ء�ƽ�ⳣ������ѧƽ��ͼ��ȣ�Ϊ��Ƶ����ͳ������ͣ����ؿ����ͼ��ķ�����ȡ��Ϣ��������һ���Ѷȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | ����±������ǿ��Ĵ���Һ�ж��ܷ�����ȥ��Ӧ | |
| B�� | ±����������ȥ��Ӧ�IJ���һ����ϩ�� | |
| C�� | ֻ��������������й����� | |
| D�� | ������������ȱ��黥Ϊͬϵ�� |
��1����֪��Fe2O3��s��+3C��ʯī��s���T2Fe��s��+3CO��g����H1
C��ʯī��s��+CO2��g���T2CO��g����H2
���H=��H1-3��H2���ú���H1����H2����ʽ��ʾ��
��2����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=64����2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⣮
| Fe2O3 | CO | Fe | CO2 | |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/mol | 1.0 | 1.5 | 1.0 | 1.0 |
������˵����ȷ����B������ĸ����
A��������ѹǿ�㶨����Ӧ�ﵽƽ��״̬
B���������������ܶȺ㶨����Ӧ�ﵽƽ��״̬
C����������CO��ƽ��ת���ʴ����ҵ�
D������Fe2O3�������CO��ת���ʣ�
CO �� g ��+2H2�� g ��?CH3OH �� l ����H
��1����֪��
| ��ѧʽ | H2��g�� | CO��g�� | CH3OH��l�� |
| ��ȼ���ȣ�25�棩 ��H/kJ•mol-1 | -285.8 | -283.0 | -726.5 |
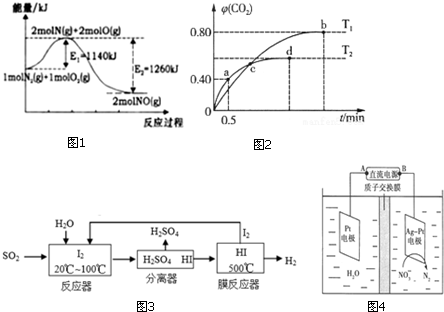
��2�����ݻ��ɱ���ܱ������г���1mol CO �� g ����2molH2�� g ������CH3OH�� g ����H2��ƽ��ת
�������¶ȣ�T����ѹǿ��P���ı仯��ͼ1��ʾ��
�ٸ÷�Ӧ�ġ�S��0��ͼ�е�T1��T2�����������������=������
�ڵ��ﵽƽ��״̬A ʱ�����������Ϊ2L����ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ4�����ﵽƽ��״̬B ʱ�������������V��B��=0.4L��
��3�����ݻ��̶�Ϊ2L���ܱ������г���2molCO�� g ����6molH2�� g ������CH3OH�� g ������Ӧʱ�������ʵ���Ũ�ȵĹ�ϵ��ͼ2��ʾ����ǰ10�����ڣ�������ƽ����Ӧ����Ϊ0.16mol•L-1•min-1����15����ʱ������ϵ�¶ȣ���20����ʱ�ﵽ��ƽ�⣬��ʱ������ת����Ϊ33.3%������ͼ2�л���15-25����c��CO���ı仯���ߣ�

| A�� | 5�� | B�� | 4�� | C�� | 3�� | D�� | 2�� |
 ��
��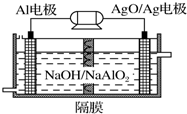 ���ǵؿ��к�����ߵĽ���Ԫ�أ��䵥�ʼ��Ͻ������������е�Ӧ�������㷺��
���ǵؿ��к�����ߵĽ���Ԫ�أ��䵥�ʼ��Ͻ������������е�Ӧ�������㷺��