题目内容
14.已知非金属单质A2、B2、C2之间能发生如下反应:A2+2B-=2A-+B2,B2+2C-=2B-+C2.以下说法正确的是( )| A. | 单质活泼性:C2>B2>A2 | B. | 还原性:A->B->C- | ||
| C. | 氧化性:A2>B2>C2 | D. | 反应:A2+2C-=2A-+C2不能发生 |
分析 氧化还原反应中氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物,标注反应过程中元素化合价变化分析判断氧化剂、还原剂、还原产物、氧化产物,利用规律分析判断.
解答 解:A2+2B-=2A-+B2,反应中A元素化合价0价变化为-1价,化合价降低做氧化剂,被还原得到还原产物A-,B元素化合价-1价变化为0价,化合价升高,做还原剂,被氧化生成氧化产物B2,得到氧化性A2>B2;同样的道理,反应B2+2C-=2B-+C2中B元素化合价0价变化为-1价,化合价降低做氧化剂,被还原得到还原产物B-,C元素化合价-1价变化为0价,化合价升高,做还原剂,被氧化生成氧化产物C2,得到氧化性B2>C2即氧化性:A2>B2>C2;
A.氧化性:A2>B2>C2,所以单质的活动性:A2>B2>C2,故A错误;
B.氧化性越强,其阴离子的还原性越弱,则还原性A-<B-<C-,故B错误;
C.由分析可知:氧化性:A2>B2>C2,故C正确;
D.氧化性:A2>C2,反应A2+2C-=2A-+C2可以证明这个氧化性顺序,所以该反应能发生,故D错误.
故选C.
点评 本题考查了氧化还原反应,侧重于氧化还原反应基本概念以及氧化性、还原性强弱比较的考查,注意把握氧化性和还原性的强弱比较方法和规律应用,题目难度中等.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 石蕊试纸和pH试纸使用前都必须用蒸馏水润湿 | |
| B. | 沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变 | |
| C. | 电离和水解反应都是吸热过程 | |
| D. | 酸式盐的pH均小于7 |
5.25℃时,测得某NH4Cl和Na2CO3溶液的pH值分别为5和10,则两溶液中水电离产生的c(H+)之比是( )
| A. | 1:10 | B. | 2:1 | C. | 105:1 | D. | 5:1 |
2.化学知识在生产和生活中有着重要的应用.下列说法中正确的是( )
①铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
②发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
③Na2O2既可作呼吸面具中O2的来源,又可漂白织物、麦杆、羽毛等
④碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑤明矾常作为消毒剂.
①铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
②发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
③Na2O2既可作呼吸面具中O2的来源,又可漂白织物、麦杆、羽毛等
④碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑤明矾常作为消毒剂.
| A. | ①②③⑤ | B. | ①②③ | C. | ①②④ | D. | ①②③④⑤ |
19.在下列溶液中,能大量共存的离子组是( )
| A. | 在强碱性溶液中能大量存在:Na+、K+、Cl-、NH4+ | |
| B. | 加入金属铝后溶液中有大量气泡产生的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| C. | 含有大量Fe3+的溶液中:SCN-、I-、K+、Br- | |
| D. | 溶液通入足量氨气后各离子还能大量存在:K+ Na+ OH-、CO32- |
3.在下列无色透明溶液中,各组离子一定能够大量共存的是( )
| A. | Al3+、Na+、Cl-、OH- | B. | Fe2+、Mg2+、SO42-、Cl- | ||
| C. | K+、Na+、CO32-、OH- | D. | Na+、Ba2+、HCO3-、OH- |
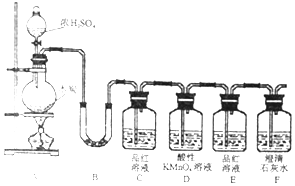
 已知:氯化铁易潮解.如图是制取无水氯化铁的实验装置图,将分液漏斗中的浓盐酸加入到盛有二氧化锰的烧瓶中,请回答下列问题:
已知:氯化铁易潮解.如图是制取无水氯化铁的实验装置图,将分液漏斗中的浓盐酸加入到盛有二氧化锰的烧瓶中,请回答下列问题: