题目内容
6.为验证浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,设计如图实验: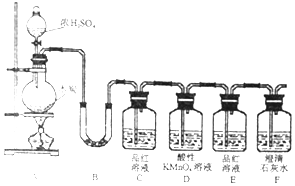
(1)写出浓硫酸与木炭粉反应的化学方程式C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O.
(2)B中加入的试剂是无水硫酸铜,现象是固体由白色变为蓝色;C的作用是验证SO2的存在,E的作用是检验SO2是否被除干净.
(3)如果将F放在B、C之间,则一定不能检出的物质是CO2.
分析 加热条件下,浓硫酸和碳反应生成二氧化碳、二氧化硫和水,B中为硫酸铜,可用于检验水的生成,C用于检验品红,D为高锰酸钾,可用于除去二氧化硫,E中品红用于检验二氧化硫是否除尽,F中澄清石灰水用于检验二氧化碳,以此解答该题.
解答 解:(1)木炭与浓硫酸再加热条件下反应生成SO2、CO2与水,反应方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O;
(2)B装置盛放试剂是无水硫酸铜,检验水蒸气,由无色变蓝色,说明含有水蒸气;C装置检验二氧化硫,E装置检验二氧化硫是否完全除尽,
故答案为:无水硫酸铜;固体由白色变为蓝色;验证SO2的存在;检验SO2是否被除干净;
(3)SO2和CO2均可以石灰水变浑浊,再结合品红溶液可以确定二氧化硫,无法检验二氧化碳,故答案为:CO2.
点评 本题考查浓硫酸性质实验,为高频考点,注意把握检验的原理,是一道综合性实验题,侧重对学生能力的考查,有利于培养学生综合分析、实验设计能力,难度中等.

练习册系列答案
相关题目
16.氯的原子序数为17,35Cl是氯的一种同位素,下列说法不正确的是( )
| A. | 35Cl原子所含质子数为18 | |
| B. | 35Cl2气体的摩尔质量为70 | |
| C. | 3.5g的35Cl2气体的体积为2.24L | |
| D. | 1/18mol的H35Cl分子所含中子数约为6.02×1023 |
17.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是 ( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物能 ⑦风能 ⑧氢能.
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物能 ⑦风能 ⑧氢能.
| A. | ①②③④ | B. | ⑤⑥⑦⑧ | C. | ③⑤⑦ | D. | ③④⑤⑥⑦⑧ |
14.已知非金属单质A2、B2、C2之间能发生如下反应:A2+2B-=2A-+B2,B2+2C-=2B-+C2.以下说法正确的是( )
| A. | 单质活泼性:C2>B2>A2 | B. | 还原性:A->B->C- | ||
| C. | 氧化性:A2>B2>C2 | D. | 反应:A2+2C-=2A-+C2不能发生 |
11.下列化合物中含2个手性碳原子的是( )
| A. | 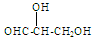 | B. | 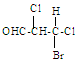 | C. |  | D. | 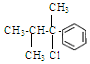 |
18.在下列溶液中,各组离了一定能够大量共存的是( )
| A. | 使酚酞试液变红的溶液中:Na+、HCO3-、NO3-、SiO32- | |
| B. | 某透明溶液中:Fe3+、K+、NO3-、Cl- | |
| C. | 某溶液中加入金属铝有氢气放出:K+、Ba2+、Cl-、SiO32- | |
| D. | 某无色溶液中:K+、Al3+、AlO2-、Cl- |
15.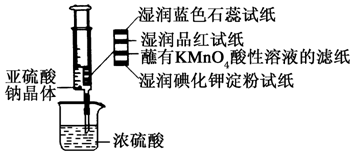 如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
 如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )| A. | 湿润的蓝色石蕊试纸先变红后褪色 | |
| B. | 湿润的品红试纸,蘸有KMnO4酸性溶液的滤纸均褪色证明了SO2的漂白性 | |
| C. | 湿润的碘化钾淀粉试纸未变蓝说明SO2氧化性强于I2 | |
| D. | 实验后,可把注射器中的物质推入NaOH溶液,以减少环境污染 |
16.下列表格中各项分类都正确的一组是( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 冰水混合物 | CuSO4•5H2O | 液态 KNO3 | 蔗糖 |
| B | CaO溶液 | 海水 | 铜 | 酒精 |
| C | 氯气 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
