题目内容
17.已知1~20号元素的离子,aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列说法正确的是( )| A. | 质子数:d>c>b>a | B. | 离子半径:W2+>X+>Y2->Z- | ||
| C. | 原子半径:Z<Y<W<X | D. | 最低负价:X<W<Z<Y |
分析 离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,则有a-2=b-1=c+2=d+1,可知原子序数a>b>d>c,W、X同周期,Y、Z同周期,且位于W、X的上一周期,
A.原子序数越大,质子数越大;
B.电子层结构相同,核电荷数越大离子半径越小;
C.电子层越多,原子半径越大,同周期从左向右原子半径减小;
D.W、X不含最低负价.
解答 解:由上述分析可知,原子序数a>b>d>c,W、X同周期,Y、Z同周期,且位于W、X的上一周期,
A.原子序数越大,质子数越大,则a>b>d>c,故A错误;
B.电子层结构相同,核电荷数越大离子半径越小,则离子半径:Y2->Z->X+>W2+,故B错误;
C.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:Z<Y<W<X,故C正确;
D.W、X不含最低负价,不能比较最低价,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、原子结构为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列有关实验原理或实验操作正确的是( )
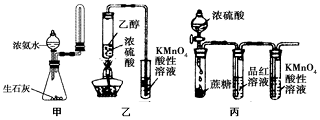

| A. | 实验室用图甲所示装置制取少量氨气 | |
| B. | 为使100ml0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50ml水 | |
| C. | 利用图乙装置,可制取乙烯并验证其易被酸性KMnO4溶液氧化 | |
| D. | 利用图丙装置,可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
8.下列实验方案中,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 验证Cl2的氧化性强于I2 | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,可观察到溶液变成蓝色 |
| B | 配制100mL 1.0mol•L-1CuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| C | 比较水与乙醇中氢的活泼性 | 分別将少量钠投入到盛有水和乙醇的烧杯中 |
| D | 验证Cu(OH)2的溶解度小于Mg(OH)2 | 将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液,可观察到先有白色沉淀生成,后变为浅蓝色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
5.下列关于有机物的叙述正确的是( )
| A. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| B. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 氯苯分子中所有原子都处于同一平面 | |
| D. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 |
12.下列实验方案中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| ① | 检验淀粉是否水解生成葡萄糖 | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后新制Cu(OH)2浊液,加热,观察是否有红色沉淀生成 |
| ② | 比较H2CO3,HCN的酸性强弱 | 用pH计测定同温度同浓度的Na2CO3溶液和NaCN溶液的pH,比较pH大小 |
| ③ | 区别植物油和矿物油 | 向植物油和矿物油中分别加入烧碱溶液,加热,冷却后观察是否分层 |
| ④ | 验证CaCO3的溶解度小于CaSO4 | 将浓Na2CO3溶液滴加到CaSO4悬浊液中,充分振荡,过滤、洗涤,向所得固体中滴加盐酸,观察是否有气体生成 |
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①③ |
3.某非金属单质气体Y2在加热条件下,1mol Y2 (g)与80克烧碱恰好完全反应,生成NaY、H2O和另一种气体,该气体是下列中的( )
| A. | H2 | B. | HY | C. | Y2 O | D. | O2 |
10.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到l.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A. | 至少存在5种离子 | |
| B. | C1-一定存在,且c Cl-)≥0.4mol/L | |
| C. | SO42-、NH4+一定存在,CO32-可能存在 | |
| D. | CO32-、Al3+一定不存在,K+一定存在 |
8.下列物质中,既可与硫酸反应,又可以与氢氧化钠溶液反应的是( )
①NaHSO4 ②Al(OH)3 ③Ca(H2PO4)2 ④(NH4)2S.
①NaHSO4 ②Al(OH)3 ③Ca(H2PO4)2 ④(NH4)2S.
| A. | 只有①②④ | B. | 只有③④ | C. | 只有②③④ | D. | 均有 |