题目内容
7.氯气泄漏事故,造成多人伤亡,附近绿地全部枯黄.翻落的氯槽罐被移至水池,除在水池里注入大量的水外还按比例注入稍过量的某化学物质A的溶液,使氯气快速与之反应,最终使事故得以控制,请根据以上事实和相关的化学知识,回答下列问题:(1)槽罐车翻倒而发生泄漏时,可以观察到的现象是空气中出现黄绿色气体;运输液氯的容器是铁槽车;氯气使人中毒的最初症状是会导致呼吸困难;在事发中心地点可采用的防护方法是BD.
A.人畜应躲到低洼的地方
B.人畜应到较高的地方
C.可用盐酸浸湿的软布蒙面
D.可用浸有苏打水的软布蒙面
(2)将泄漏的液氯罐淹没到水池中,观察到水池中的“水”呈淡黄绿色;其中含有的物质有Cl2(填化学式);注入稍过量的物质A的溶液,观察到水池里的“水”的颜色变化是淡黄绿色褪去;反应的化学方程式为Cl2+2OH-=Cl-+ClO-+H2O.
分析 氯气泄漏事故,造成多人伤亡,附近绿地全部枯黄.翻落的氯槽罐被移至水池,除在水池里注入大量的水外还按比例注入稍过量的某化学物质A的溶液,使氯气快速与之反应,最终使事故得以控制,氯气和碱溶液发生反应,所以A溶液为稀氢氧化钠溶液,
(1)氯气是黄绿色气体,常温下氯气和铁不发生反应,氯气是一种黄绿色的有毒气体,密度比空气大,能溶于水,并能与碱反应.氯气被吸入人体后,会导致呼吸困难,甚至窒息死亡;
(2)氯气呈黄绿色,氯气溶于水,部分氯气和水反应生成盐酸和次氯酸,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水.
解答 解:(1)槽罐车翻倒而发生泄漏时,可以观察到的现象是空气中出现黄绿色气体,常温下氯气和铁不发生反应,运输液氯的容器是铁槽车,氯气有毒,人吸入后氯气使人中毒的最初症状是会导致呼吸困难,在事发中心地点可采用的防护方法是,
A.氯气密度比空气重,人畜不应躲到低洼的地方,故A错误;
B.氯气密度比空气重,人畜应到较高的地方,故B正确;
C.盐酸是强酸具有腐蚀性,不可用盐酸浸湿的软布蒙面,故C错误;
D.苏打水碱性弱和氯气能发生反应,可用浸有苏打水的软布蒙面,故D正确;
故答案为:空气中出现黄绿色气体,铁槽车,会导致呼吸困难,BD;
(2)氯气呈黄绿色,氯气溶于水,水溶液呈淡黄绿色,注入稍过量的物质A的溶液,观察到水池里的“水”的颜色变化是淡黄绿色颜色褪去,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O
故答案为:淡黄绿;Cl2;淡黄绿色颜色褪去;Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题考查了探究氯气、氯水的漂白性,氯气的化学性质,题量较大,涉及内容较多,题目难度中等.

练习册系列答案
相关题目
17.下列物质中,属于电解质的是( )
| A. | 铜 | B. | 氯化钠溶液 | C. | 酒精 | D. | 烧碱 |
18.关于氨的下列叙述中,正确的是( )
| A. | 氨具有还原性,可以被氧化为NO | |
| B. | 氨因为有刺激性气味,因此不用来作制冷剂 | |
| C. | 氨极易溶于水,因此氨水比较稳定(不容易分解) | |
| D. | 氨溶于水显弱碱性,因此可使石蕊试液变为红色 |
15.A、B、X、Y、Z、W六种短周期主族元素,A是地壳中含量最多的金属元素,短周期主族元素中B的原子半径最大,X、Y、Z、W元素在周期表中的相对位置如图所示,其中Z元素原子最外层电子数是电子层数的2倍.请回答下列问题:
(1)W的最高价氧化物化学式是Cl2O7;Z的原子结构示意图为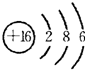 .
.
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂 c.将X的简单气态氢化物及时移离
d.增大反应体系的压强
(5)标准状况下,2.24L X的简单气态氢化物被100mL l.0mol•L-1X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-);.
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
| X | Y | |
| Z | W |
 .
.(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂 c.将X的简单气态氢化物及时移离
d.增大反应体系的压强
(5)标准状况下,2.24L X的简单气态氢化物被100mL l.0mol•L-1X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-);.
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
12.W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,X是地壳中含量最多的元素,由此可知( )
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素氧化物对应水化物的酸性一定强于Y | |
| C. | X元素形成的单核阴离子还原性强于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
19.短周期元素X、Y、Z、W的原子序数依次增大,X原子在元素周期表中原子半径最小,Y的次外层电子数是最外层的$\frac{1}{3}$,ZX2是一种储氢材料,W与Y属于同一主族.下列叙述正确的是( )
| A. | 原子半径:rW>rZ>rY | |
| B. | 化合物X2Y、ZY、ZX2中化学键的类型相同 | |
| C. | 由X、Y、Z、W组成的化合物的水溶液可能显酸性 | |
| D. | 由Y元素形成的离子与W元素形成的离子的电子数不可能相同 |
16.下列有关物质的性质与应用的说法均正确,且具有因果关系的是( )
| A. | 氯气有毒,不可用于自来水的杀菌消毒 | |
| B. | Al(OH)3受热分解生成H2O并吸收大量的热量,可用作阻燃剂 | |
| C. | 二氧化硅不与强酸反应,可用玻璃容器盛放氢氟酸 | |
| D. | Na2O2具有强氧化性,可用作呼吸面具的供氧剂 |
 ⑥
⑥