题目内容
18.关于氨的下列叙述中,正确的是( )| A. | 氨具有还原性,可以被氧化为NO | |
| B. | 氨因为有刺激性气味,因此不用来作制冷剂 | |
| C. | 氨极易溶于水,因此氨水比较稳定(不容易分解) | |
| D. | 氨溶于水显弱碱性,因此可使石蕊试液变为红色 |
分析 A.依据氨气中氮元素化合价判断氨气的性质;
B.液态氨气汽化需要吸收大量的热,氨气具有制冷作用;
C.依据一水合氨的不稳定性解答;
D.石蕊试液遇到碱变蓝色.
解答 解:A.氨气中氮元素处于最低价-3价,化合价能够升高为一氧化氮中的+2价,所以氨气能够被氧化生成一氧化氮,故A正确;
B.液态氨气汽化需要吸收大量的热,氨气具有制冷作用,常用作制冷剂,故B错误;
C.一水合氨不稳定,受热易分解,故C错误;
D.氨溶于水显弱碱性,因此可使石蕊试液变为蓝色,故D错误;
故选:A.
点评 本题考查了元素化合物知识,熟悉氨气的性质是解题关键,注意氨气催化氧化生成一氧化氮,为工业制备硝酸的重要反应,题目难度不大.

练习册系列答案
相关题目
9.含镁离子和铝离子个数比为1:2的氯化镁和氯化铝两种溶液,若使溶液中的氯离子完全沉淀,用去相同浓度的硝酸银溶液的质量比为( )
| A. | 1:3 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
13.银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O═2Ag+Zn(OH)2,下列说法中不正确的是( )
| A. | 原电池放电时,负极上发生反应的物质是Zn | |
| B. | 负极发生的反应是Zn+2OH--2e-═Zn(OH)2 | |
| C. | 工作时,负极区溶液碱性减弱,正极区溶液碱性增强 | |
| D. | 溶液中OH-向正极移动,K+、H+向负极移动 |
3.胶体区别于其它分散系的本质是( )
| A. | 胶体粒子带电荷并且在一定条件下能稳定存在 | |
| B. | 胶体的分散质粒子直径在1nm~100nm之间 | |
| C. | 胶体粒子不能穿过半透膜,能通过滤纸空隙 | |
| D. | 胶体粒子能够发生布朗运动而且能产生丁达尔现象 |
10.下图所示的实验操作,不能达到实验目的是( )
| A. | 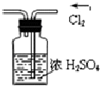 干燥Cl2 | B. | 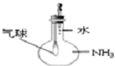 证明氨气极易溶于水 | ||
| C. |  检验K2CO3中的K+ | D. |  实验室制取氨气 |
 ⑤
⑤

 .
.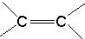 )中的π-键不能自由旋转,因此
)中的π-键不能自由旋转,因此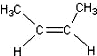 和
和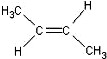 是两种不同的化合物,互为顺反异构体.则分子式为C3H4Cl2的化合物的烯烃异构体有( )
是两种不同的化合物,互为顺反异构体.则分子式为C3H4Cl2的化合物的烯烃异构体有( )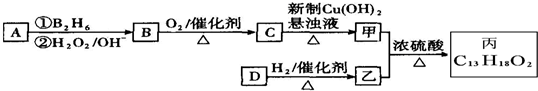
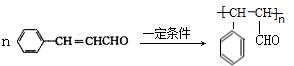 .
. .
. .
.