题目内容
2.A、B、C是含有同一种元素的三种气体,A无色,在一定条件下可以被空气中的氧气氧化为B和另一种中性物质;B不溶于水,但遇到空气即迅速转化为C;A、C均易溶于水,二者水溶液的酸、碱性正好相反,C与水反应后所得的物质与A相遇可产生大量白烟状物质D,由此推断:(1)写出A、B、C的化学式:ANH3 BNO CNO2
(2)A在一定条件下转变为B的化学方程式为:4NH3+5O2$\frac{\underline{\;一定条件下\;}}{\;}$4NO+6H2O
(3)C物质和水反应的化学方程式为:3NO2+H2O═2HNO3+NO
(4)D中阳离子的电子式:
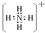 .
.
分析 A、B、C是含有同一种元素的三种气体,A无色,在一定条件下可以被空气中的氧气氧化为B和另一种中性物质;B不溶于水,但遇到空气即迅速转化为C;A、C均易溶于水,二者水溶液的酸、碱性正好相反,C与水反应后所得的物质与A相遇可产生大量白烟状物质D,能与空气在常温下反应的气体有NO,如果B是NO,则C是NO2、A是NH3、D是NH4NO3,通过检验符合题意,再结合题目分析解答.
解答 解:A、B、C是含有同一种元素的三种气体,A无色,在一定条件下可以被空气中的氧气氧化为B和另一种中性物质;B不溶于水,但遇到空气即迅速转化为C;A、C均易溶于水,二者水溶液的酸、碱性正好相反,C与水反应后所得的物质与A相遇可产生大量白烟状物质D,能与空气在常温下反应的气体有NO,如果B是NO,则C是NO2、A是NH3、D是NH4NO3,通过检验符合题意,
(1)A、B、C的化学式分别为:NH3、NO、NO2,
故答案为:NH3;NO;NO2;
(2)A是氨气、B是NO,氨气和氧气在一定条件下反应生成NO和水,反应方程式为4 NH3+5O2$\frac{\underline{\;一定条件下\;}}{\;}$4NO+6H2O,
故答案为:4 NH3+5O2$\frac{\underline{\;一定条件下\;}}{\;}$4NO+6H2O;
(3)C是二氧化氮,二氧化氮和水反应生成硝酸和NO,C物质和水反应的化学方程式为:3NO2+H2O═2HNO3+NO,故答案为:3NO2+H2O═2HNO3+NO;
(4)D是硝酸铵,硝酸铵中铵根离子中N、H原子之间共用一对电子对,D中阳离子的电子式: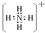 ,
,
故答案为: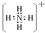 .
.
点评 本题考查无机物推断,为高频考点,侧重考查学生分析推断能力,明确物质之间的转化及物质性质是解本题关键,以A、C易属于水且二者水溶液的酸、碱性正好相反为突破口进行推断,题目难度中等.

| A. | a=b=c | B. | a>b>c | C. | b>c>a | D. | c>b>a |
| A. | H2O | B. | SO3 | C. | NaH | D. | NH3 |
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 碳酸钠溶液中加入足量盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
①“白雪牌”漂粉精可令所有有色物质黯然失“色”,没有最白,只有更白
②霸王洗发液不含任何化学物质
③夏天混用不同品牌的墨水书写时,钢笔的笔尖容易发生堵塞是因为胶体发生了聚沉的原因
④53度白酒是指该白酒的着火点是53℃
⑤太太口服液含丰富的氮、磷、锌等微量元素.
则有关上述说法,你的看法是( )
| A. | 全部正确 | B. | 只有①⑤正确 | ||
| C. | 只有③正确 | D. | 以上说法都是错误的 |
| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+═H2SiO3↓ | |
| C. | 0.01 mol/L NH4Al(SO4)2溶液与0.02 mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
| A. | CuSO4 | B. | KCl | C. | H2SO4 | D. | Na2SO4 |