��Ŀ����
��ͼ����װ���У�Һ�������Ϊ200 mL����ʼ����ǰ�������Һ��Ũ�Ⱦ�Ϊ0.5 mol/L������һ��ʱ������0.02 mol����ͨ������������Һ����ı仯

����������ȷ����
A������������� ��=��
B�����������������ӣ���������������С
C����Һ��pH�仯���ټ�С��������
D���缫��Ӧʽ������������4OH�� - 4e�� = 2H2O+O2�� ���и�����2H++2e��=H2��
C
��������
���������A�����ǵ��أ������ֱ����Cu��������������Cu2++2e-==Cu ��������2H2O -4e- =O2��+4H+����ͨ��0.02mol����ʱ����������0.02mol/4=0.005mol������ԭ��أ�Zn������������Zn-2e-=Zn2+��Cu������������2H++2e-==H2������ͨ��0.02mol����ʱ���������������ʵ�����0.01mol������ڲ��������岻��ȣ�����B������������Cu�������������ӣ����������������������������缫�������䣬����C�����������������ӷŵ磬���������������ӣ�������ҺpH��С�����������ӷŵ���������������������Ũ������������ҺpH������ȷ��D������ԭ��أ�Zn������������Zn-2e-=Zn2+������ѡC��
���㣺����ԭ��ء����ص��жϣ���Ӧԭ����Ӧ��

(14��)�⻯��(CaH2)�Ƕ��ֳ��õĴ�����ϣ�Ҳ�ǵ�ɽ�˶�Ա���õ���Դ�ṩ������Ҫ�ܷⱣ�棬��ˮ��Ӧ�����������ƺ�������ij�о���ѧϰС��ģ��������ҵ��ȡ�⻯�ơ�
��ʵ�顿
��п����ϡ���ᷴӦ�Ƶø������������������������ڼ��ȵ�������ֱ�ӻ��ϣ������Ƶ�CaH2��
��1�������йظ�ʵ���˵����ȷ���� ��
a������������ͬʱ����п��ȡ���������ʱȴ�п��
b������ʱ������ͨ�뵪����Ϊ���������Է�ֹ�����ĸ���
c��������Ũ������ʯ�Ҷ�H2���и������
d����ʼʵ��ʱ��Ӧ��ͨ��H2����������Ƽ���
e����ֹͣʵ��ʱ��Ӧ��ֹͣͨ��H2����ֹͣ���ȡ�
��������衿
��2������ʵ���в��������������ƻ��⻯�ƶ����ܱ���������С���ͬѧ�Է�Ӧ��Ĺ������ɷ�������¼��衣
����l������Ca ��CaH2��
����2������CaH2��CaO��
����3������ ��
�����ʵ�鷽������֤���衿
��3������ʵ���û�ѧ��������Ca��CaH2�������ʵ������±������ݡ�
ʵ�鲽��(��Ҫ��д�����������) | Ԥ������ͽ��� |
ȡ����������Ʒ���� |
��4������ʵ�� �ⶨCa ��CaH2 �������CaH2 ������������
��ȡm1g��Ʒ��ˮ��ȫ��Ӧ��������ͼװ�òⶨ���ɵ��������ʱ���� ʱ�����ռ�������ĸ��
a���տ�ʼ������ʱ b��������������ʱ c�����徭���鴿�����ռ�

�����װ�����������ã�������ȷ����ͬѧ��Ϊ������Һ����룬�������������ⶨƫ���������⻯�Ƶ��������� ���조ƫ�ߡ�����ƫ�͡�����Ӱ�족��
����˼�뽻����
��5����ɽ�˶�Ա�����⻯����Ϊ��Դ�ṩ������������ȣ����ŵ����⻯���ǹ��壬Я�����㡣��Ȼ��������ˮ��ӦҲ������������Ϊʲô��Ҫ���������Ʊ����⻯���أ���Ĺ۵��� ��
��12�֣�
��1��20��ʱ0.1 mol��L��1NaOH�ֱ�ζ�0.1 mol��L��1HCl��0.1 mol��L��1CH3COOH��pH�仯�������¡�
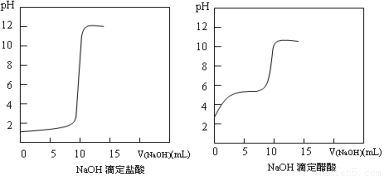
�����������ش��������⣺
�ٲ�ô������pHΪ3����20��ʱ��Ũ�ȴ���ĵ����Ϊ ��
�ڵζ���ʼ��������߱仯��������ԭ���� ��
��2��25 ��ʱ0.1 mol��L-1��H2Rˮ��Һ�У�������������������ҺpH���õ�����H2R��HR����R2������������Һ����c(Na+)=c(R2��)+c(HR��)+c(H2R)ʱ��Һ������Ϊ (�ѧʽ)��
��3����ͼ��ijˮ��Һ��pH��0��14�ķ�Χ��H2CO3��HCO3����CO32�����ֳɷ�ƽ��ʱ����ɷ�����
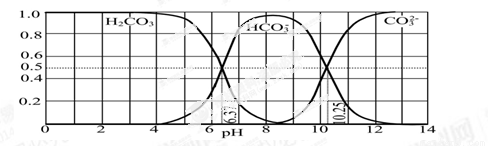
������������ȷ���� ��
A����ͼ��1.0 mol��L��1̼������Һ�ζ�1.0 mol��L��1 HCl��Һ�ĵζ�����
B����pH�ֱ�Ϊ6.37��10.25ʱ����Һ��c(H2CO3)=c(HCO3��)=c(CO32��)
C������ѪҺ��pHԼΪ7.4����CO2��ѪҺ�ж���HCO3����ʽ����
D������CO2��NaOH��Ӧ��ȡNaHCO3���˿�����Һ��pHΪ7��9֮��
��4��������ʩ����������ͨ��ת��Ϊ̼��炙�̼����狀�ű����������ã����ط�����������ڵ���ø�����£�ת��Ϊ̼��李���֪���������ˮ�еĵ���ƽ�ⳣ����25�棩���±���
������� | H2CO3 | NH3��H2O |
����ƽ�ⳣ�� | Ka1��4.30��10-7 Ka2��5.61��10-11 | 1.77��10-5 |
���г�����0.1 mol��L-1��(NH4)2CO3��Һ��
������Ϊ����Һ�� �ԣ���ᡱ�����С����������ԭ���� ��
�ھ���Һ������֮�������й�ϵʽ������Ϊ������ȷ���� ��
A��c (NH4+)��c (CO32-)��c (HCO3-)��c (NH3��H2O)
B��c(NH4+)+c(H+)��c(HCO3-)+c(OH-)+c(CO32-)
C��c (CO32-) + c (HCO3-) +c (H2CO3)��0.1 mol��L-1
D��c (NH4+)+ c (NH3��H2O)��2 c (CO32-) + 2c (HCO3-) +2 c (H2CO3)
 CH3OCH3��g��+3H2O��g�� ��H��0
CH3OCH3��g��+3H2O��g�� ��H��0
 ��HCl��aq����NaOH��aq�� �� Ӧ��
��HCl��aq����NaOH��aq�� �� Ӧ�� ����HCN��ˮ��Һ�е����
����HCN��ˮ��Һ�е����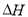 ����
����
 B��-43.5
B��-43.5


 KOH��H2��+I2
KOH��H2��+I2 CO����CO2������x+1��H2O�������ɵ�CO2��ˮ�������������õ��ϴ�����CO���塣
CO����CO2������x+1��H2O�������ɵ�CO2��ˮ�������������õ��ϴ�����CO���塣