��Ŀ����
��15�֣����ѣ�CH3OCH3������Ϊ21���͵�����ȼ�ϣ�����ࡢ��Ч�����������Ļ������ܣ�������һ����ɫ���壬������������ζ����ȼ����Ϊ1455 kJ��mol�����ѿ���ȼ�ϵ�ص�ȼ�ϡ�
��1��д������ȼ�յ��Ȼ�ѧ����ʽ ����֪H2��g����C��s����ȼ���ȷֱ���285.8 kJ��mol-1��393.5 kJ��mol-1�����㷴Ӧ4C��s��+6H2��g��+O2��g��==2CH3OCH3 ��g���ķ�Ӧ��Ϊ ��
��2����ҵ������H2��CO2�ϳɶ����ѵķ�Ӧ���£�6H2��g��+2CO2��g�� CH3OCH3��g��+3H2O��g�� ��H��0
CH3OCH3��g��+3H2O��g�� ��H��0
��һ���¶��£���һ���̶�������ܱ������н��и÷�Ӧ���������жϷ�Ӧ�ﵽ��ѧƽ��״̬����
______��ѡ���ţ�ע���Сд��
a��c��H2����c��H2O���ı�ֵ���ֲ���
b����λʱ������2mol H2����ʱ��1mol H2O����
c�������������ܶȲ��ٸı�
d������������ѹǿ���ٸı�
���¶����ߣ��û�ѧƽ���ƶ����µ�ƽ�⣬CH3OCH3�IJ��ʽ�
________����������С�����䡱����ͬ������������ƽ��ʽ����__________��
��3���Լ��ѡ�����������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�ء��õ�صĸ�����ӦʽΪ____________________��
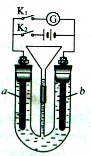
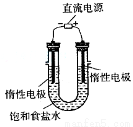
��4���ã�3���е�ȼ�ϵ��Ϊ��Դ����ʯīΪ�缫���500 mL���з�̪��NaCl��Һ��װ����ͼ��ʾ��

��д����������Y�缫�����۲쵽������ ����ȼ�ϵ������2.8 LO2����״���£�ʱ�������ʱ��NaCl��Һ��pH= ��������Һ��������䣬����ȫ������Һ���ݳ�����
��1��CH3OCH3��g��+3O2��g��=2CO2��g��+3H2O��l�� ��H= ��1455kJ/mol��2�֣�
��H=��378.8kJ/mol��3�֣� ��2����a d������1�֣���2�֣��� ��С����С������1�֣���2�֣�
��3��CH3OCH3+16OH����12e-��2CO32-+11H2O��2�֣�
��4��Y�缫������Һ��������������ϲ��ֳʻ���ɫ��2�֣� 14��2�֣�
��������
�����������1��ȼ��������һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų������������ѵ�ȼ����Ϊ1455 kJ��mol�������ȼ�յ��Ȼ�ѧ����ʽΪCH3OCH3��g��+3O2��g��=2CO2��g��+3H2O��l�� ��H= ��1455kJ/mol����֪H2��g����C��s����ȼ���ȷֱ���285.8 kJ��mol-1��393.5 kJ��mol-1�����йص��Ȼ�ѧ����ʽΪ����H2��g��+1/2O2��g����H2O��l����H����285.8KJ/mol����C��s��+O2��g����CO2��g����H����393.5KJ/mol����CH3OCH3��g��+3O2��g����2CO2��g��+3H2O��l����H����1455kJ/mol�����Ը��ݸ�˹���ɿ�֪�١�3+�ڡ�2-�۵õ���Ӧ�Ȼ�ѧ����ʽΪ��2C��s��+3H2��g��+1/2O2��g����CH2OCH3��g�� ��H����169.4kJ/mol����4C��s��+6H2��g��+O2��g����2CH2OCH3��g�� ��H����378.8kJ/mol��
��2������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬��A�������Ƿ�Ӧǰ��ˮ�������������˵�c��H2����c��H2O���ı�ֵ���ֲ���ʱ����˵����Ӧ�ﵽƽ��״̬��a��ȷ��b�����ݷ���ʽ��֪��λʱ������2mol H2����ʱһ����1mol H2O���ɣ���˲��ܾݴ�˵���ﵽƽ��״̬��b����c���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ���������������ܶȲ��ٸı䲻��˵���ﵽƽ��״̬��c����D������Ӧ��ѹǿ��С�Ŀ��淴Ӧ����˵�����������ѹǿ���ٸı�����˵���ﵽƽ��״̬��d��ȷ����ѡad��
������Ӧ�Ƿ��ȷ�Ӧ������¶����ߣ��û�ѧƽ�����淴Ӧ�����ƶ��������µ�ƽ�⣬CH3OCH3�IJ��ʽ���С���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ���������䣬���ʵ����������������ƽ��ʽ������С��
��3��ԭ��ظ���ʧȥ���ӣ�����������Ӧ����˼����ڸ����ŵ磬��������������̼���������ˮ����缫��ӦʽΪCH3OCH3+16OH����12e-��2CO32-+11H2O��
��4������װ��ͼ��֪Y�缫���Դ����������������������Һ�е������ӷŵ��������������Y�缫������Һ��������������ϲ��ֳʻ���ɫ����״����2.8LO2�����ʵ�����2.8L��22.4L/mol��0.125mol�����ݵ缫��ӦO2+2H2O+4e-��4OH-��֪����ת��Ϊ0.125mol��4��0.5mol�����Ը��ݵ����غ��֪������Ҳת��0.5mol���ӣ���˸��������缫��ӦΪ4OH--4e-��2H2O+O2����֪�������������ӵ����ʵ�����0.5mol����Ũ����0.5mol��0.5L��1.0mol/L��������Һ��������Ũ����10��14mol/L�������Һ��pH��14��
���㣺����ȼ���ȡ��Ȼ�ѧ����ʽ����˹���ɡ�ƽ��״̬�жϡ����������ƽ��״̬��Ӱ���Լ��绯ѧԭ����Ӧ�õ�

 ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�