题目内容
15.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的:①NaOH固体 ②H2O ③NaCl固体 ④CH3COONa固体 ⑤KCl溶液( )| A. | ②④⑤ | B. | ①②③ | C. | ①③⑤ | D. | ②③④ |
分析 Fe过量,生成氢气由盐酸决定,为了减缓反应速度,且不影响生成氢气的总量,减小氢离子浓度不改变其物质的量即可,以此来解答.
解答 解:①NaOH固体,与盐酸反应,生成氢气的量减少,故不选;
②H2O,对盐酸稀释,氢离子浓度减小但物质的量不变,故选;
③NaCl固体,对反应无影响,故不选;
④CH3COONa固体,生成醋酸,氢离子浓度减小但物质的量不变,故选;
⑤KCl溶液,相当于对盐酸稀释,氢离子浓度减小但物质的量不变,故选;
故选A.
点评 本题考查影响化学反应速率的因素,明确浓度对反应速率的影响即可解答,注意Fe过量,改变浓度是关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列物质①NaHCO3 ②Al(OH)3 ③Al ④Al2O3中,跟盐酸和氢氧化钠溶液都能反应的是( )
| A. | 只有②④ | B. | 只有①② | C. | 只有①②③ | D. | ①②③④ |
13.我国的《能源百科全书》说:“能源是可以直接或经转换提供给人类所需的光、热、动力等任一形式的、且可以互相转换的能量的源泉.”人类对于能源的利用大致可以分为三个时代:柴草能源、化石能源、多能源时代.以下说法正确的是( )
| A. | 原始社会人类学会利用火,他们以天然气取暖,吃熟食,从事生产活动 | |
| B. | 多年来我国广大农村生火做饭使用的都是化石燃料 | |
| C. | 多能源时代指的是新能源时代,包括核能、太阳能、氢能 | |
| D. | 化石燃料的燃烧没有污染 |
10.下列各组物质充分反应后,只能得到一种气体的是( )
| A. | 木炭和浓硫酸共热 | B. | 过氧化钠与足量的稀硫酸反应 | ||
| C. | 足量的铜与一定量的浓硝酸反应 | D. | 足量的锌和定量的浓硫酸反应 |
20.氰化物有剧毒,我国工业废水中氰化物(CN-)的处理方法是:在碱性条件下,用Cl2将废水的中CN-转化成N2和CO2等,使废水得到净化.发生的反应为:2CN-+8OH-+5Cl2═2CO2↑+N2↑+10Cl-+4H2O.下列有关说法正确的是( )
| A. | 上述反应中氧化产物只有N2 | |
| B. | 经测定,NaCN的水溶液呈碱性,说明CN-能促进水的电离 | |
| C. | 若上述反应生成0.4molCO2,则溶液中阴离子增加的物质的量为2mol | |
| D. | 现取1L含CN-1.04mg/L的废水,理论需用4.010-5molCl2处理 |
7.为体现“绿色奥运”“科技奥运”,2008年北京奥运会出现了中国自己生产的燃料电池汽车,作为马拉松领跑车和电视拍摄车,该车装着“绿色心脏”--质子交换膜燃料电池,下列叙述正确的是( )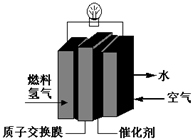

| A. | 总反应式为:O2+2H2═2H2O | |
| B. | 正极的电极反应式为:O2+4H+═2H2O+4e- | |
| C. | 通入氧气的电极发生氧化反应 | |
| D. | 通入氢气的电极为正极 |

 .
. CH4、NH3、H2O和HF均为含10e-的分子.
CH4、NH3、H2O和HF均为含10e-的分子.