题目内容
1.下列物质反应后的溶液中加入KSCN溶液一定会变红色的( )| A. | Fe2O3与HCl反应 | B. | 过量铁粉与稀硝酸反应 | ||
| C. | 少量铁粉与稀盐酸作用 | D. | 铁粉与CuSO4反应 |
分析 反应后的溶液中滴加KSCN溶液变红色,说明反应溶液中存在铁离子,以此来解答.
解答 解:A.反应后生成氯化铁,KSCN溶液变红色,故A正确;
B.铁过量,反应生成硝酸亚铁,加KSCN溶液不变红色,故B错误;
C.反应生成氯化亚铁,加KSCN溶液不变红色,故C错误;
D.反应生成硫酸亚铁,加KSCN溶液不变红色,故D错误;
故选A.
点评 本题考查铁的化学性质,为高频考点,把握发生的氧化还原反应及产物中铁的化合价为解答的关键,注意Fe与铁离子、铁离子及非氧化性酸反应生成亚铁离子,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A. | CO2的电子式: | B. | 8个中子的碳原子的符号:12C | ||
| C. | 次氯酸分子的结构式:H-O-Cl | D. | 乙烯的结构简式:CH2CH2 |
12.在实验室中,对下列事故或药品的处理正确的是( )
| A. | 含硫酸的废液倒入水槽,用水冲入下水道 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 温度计不慎打破,散落的水银应用硫粉处理后收集 |
10.某溶液可能含有Cl-、SO42-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH 溶液,加热,得到0.02mol 气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6g 固体;向上述滤液中加足量BaCl2溶液,得到 4.66g 不溶于盐酸的沉淀.由此可知原溶液中( )
| A. | 至少存在5 种离子 | |
| B. | SO42-、NH4+、Fe3+、一定存在,Cl-、K+、Al3+可能存在 | |
| C. | K+一定存在,Al3+可能存在 | |
| D. | Cl-一定存在,且c(Cl-)≥0.4mol/L |
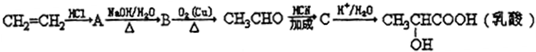
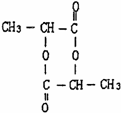 、两分子成链状酯
、两分子成链状酯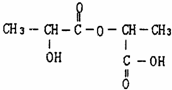 .
.