题目内容
下列物质既属于钾盐又属于硫酸盐的是( )
| A、碳酸钾 | B、硫酸钠 |
| C、碳酸钠 | D、硫酸钾 |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:盐是指含有金属离子(铵根)和酸根离子的化合物,可根据所含有的金属或酸根去命名,钾盐指由钾离子和酸根离子构成的盐,硫酸盐指金属离子(铵根)和硫酸酸根离子构成的盐.
解答:
解:钾盐指由钾离子和酸根离子构成的盐,所以Na2CO3、Na2SO4都属于钠盐,K2SO4、K2CO3属于钾盐;
硫酸盐指金属离子(铵根)和硫酸酸根离子构成的盐,Na2SO4、K2SO4属于硫酸盐;Na2CO3,K2CO3 属于碳酸盐;
所以既属于钠盐又属于硫酸盐的是K2SO4,
故选:D.
硫酸盐指金属离子(铵根)和硫酸酸根离子构成的盐,Na2SO4、K2SO4属于硫酸盐;Na2CO3,K2CO3 属于碳酸盐;
所以既属于钠盐又属于硫酸盐的是K2SO4,
故选:D.
点评:本题主要考查了盐的分类,正确理解盐的定义、盐的分类是解题的前提,难度不大.

练习册系列答案
相关题目
下列离子中,不可能与H+大量共存于同一溶液中的是( )
A、S
| ||
| B、Cl- | ||
| C、Cu2+ | ||
D、N
|
用MnO2和浓盐酸制取氯气,当4mol氯化氢被氧化时,生成的氯气的体积(标况)是( )
| A、22.4L |
| B、44.8L |
| C、67.2L |
| D、89.6L |
下列对碱金属的叙述,其中完全不正确的组合是( )
①K通常保存在煤油中,以隔绝与空气的接触;
②碱金属常温下呈固态,取用时可直接用手拿;
③碱金属中还原性最强的是钾;
④碱金属阳离子,氧化性最强的是Li+;
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大;
⑥从Li到Cs,碱金属的密度越来越大,熔沸点越来越高.
①K通常保存在煤油中,以隔绝与空气的接触;
②碱金属常温下呈固态,取用时可直接用手拿;
③碱金属中还原性最强的是钾;
④碱金属阳离子,氧化性最强的是Li+;
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大;
⑥从Li到Cs,碱金属的密度越来越大,熔沸点越来越高.
| A、②③⑥ | B、②③④ |
| C、④⑤⑥ | D、①③⑤ |
下列说法正确的是( )
| A、H2的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为142.9kJ?g-1,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ?mol-1 |
| B、反应A(g)═2B(g),若正反应的活化能为Ea kJ?mol-1,逆反应的活化能为Eb kJ?mol-1,则△H=(Ea-Eb)kJ?mol-1 |
| C、能自发进行的化学反应,一定是△H<0、△S>0 |
| D、增大反应物浓度,可增大单位体积内活化分子百分数,从而增加有效碰撞的次数 |
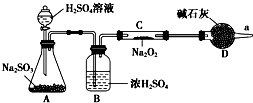 ①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).
①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).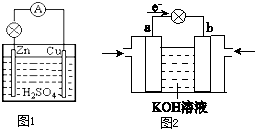 原电池是直接把化学能转化为电能的装置.
原电池是直接把化学能转化为电能的装置.