题目内容
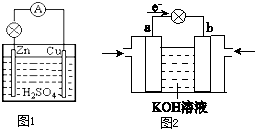 原电池是直接把化学能转化为电能的装置.
原电池是直接把化学能转化为电能的装置.(1)如图1所示:在Cu-Zn原电池中,Zn极发生
(2)航天技术上使用的氢-氧燃料电池具有高能、轻便和不污染环境等优点.其放电时的电池总反应方程式为:2H2+O2=2H2O.
图2是氢-氧燃料电池的装置图.则:
①溶液中OH-移向
②b电极周围通入的气体为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)Cu-Zn原电池中Zn在负极发生氧化反应,Zn失电子生成Zn2+;Cu为正极,正极上氢离子得电子,生成氢气;
(2)原电池中电子从负极流向正极;溶液中阴离子向负极移动;氢-氧燃料电池中氧气在正极上得电子生成氢氧根离子.
(2)原电池中电子从负极流向正极;溶液中阴离子向负极移动;氢-氧燃料电池中氧气在正极上得电子生成氢氧根离子.
解答:
解:(1)Cu-Zn原电池中Zn在负极发生氧化反应,Zn失电子生成Zn2+,其电极反应为:Zn-2e-=Zn2+;Cu为正极,正极上氢离子得电子,生成氢气,其电极反应为:2H++2e-=2H2↑;
故答案为:氧化;Zn-2e-=Zn2+;正;2H++2e-=2H2↑;
(2)①原电池中电子从负极流向正极,已知图中电子从a流向b,则a 为负极,b为正极;溶液中阴离子向负极移动,则溶液中OH-移向a,
故答案为:a;
②氢-氧燃料电池中氧气在正极上得电子,即O2在b电极反应生成氢氧根离子,其电极反应式为:O2+2H2O+4e-=4OH-,故答案为:O2;O2+2H2O+4e-=4OH-.
故答案为:氧化;Zn-2e-=Zn2+;正;2H++2e-=2H2↑;
(2)①原电池中电子从负极流向正极,已知图中电子从a流向b,则a 为负极,b为正极;溶液中阴离子向负极移动,则溶液中OH-移向a,
故答案为:a;
②氢-氧燃料电池中氧气在正极上得电子,即O2在b电极反应生成氢氧根离子,其电极反应式为:O2+2H2O+4e-=4OH-,故答案为:O2;O2+2H2O+4e-=4OH-.
点评:本题考查了原电池原理的应用,注意把握导线中电子的移动方向及溶液中离子的移动方向,明确电极方程式的书写方法是解决本题的关键,题目难度中等.

练习册系列答案
相关题目
下列物质既属于钾盐又属于硫酸盐的是( )
| A、碳酸钾 | B、硫酸钠 |
| C、碳酸钠 | D、硫酸钾 |
常温常压下,1g H2在足量Cl2中燃烧生成HCl气体,放出 92.3kJ的热量,则该反应的热化学方程式书写正确的是( )
| A、H2(g)+Cl2(g)=2HCl(g);△H=-92.3 kJ/mol |
| B、H2(g)+Cl2(g)=HCl(g);△H=+92.3kJ/mol |
| C、2HCl=H2+Cl2;△H=+184.6kJ/mol |
| D、H2 (g)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol |
下列各组反应中,第一个反应放出的热量比第二个反应放出的热量多的是(g、l、s分别表示气体、液体、固体)( )
| A、2H2(g)+O2(g)=2H2O(1)2H2(g)+O2(g)=2H2O(g) | ||||
B、
| ||||
C、C(s)+
| ||||
| D、S(s)+O2(g)=SO2(g) S(g)+O2(g)=SO2(g) |
进入2013年以来,我国中东部地区曾出现严重的雾霾天气.下列有关防治雾霾天气的说法不正确的是( )
| A、开发利用太阳能、生物质能等清洁能源 |
| B、研制开发燃料电池汽车 |
| C、积极发展公共交通,倡导绿色出行 |
| D、充分开发利用纯天然纤维,停止使用各种化学合成材料 |