题目内容
下列对碱金属的叙述,其中完全不正确的组合是( )
①K通常保存在煤油中,以隔绝与空气的接触;
②碱金属常温下呈固态,取用时可直接用手拿;
③碱金属中还原性最强的是钾;
④碱金属阳离子,氧化性最强的是Li+;
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大;
⑥从Li到Cs,碱金属的密度越来越大,熔沸点越来越高.
①K通常保存在煤油中,以隔绝与空气的接触;
②碱金属常温下呈固态,取用时可直接用手拿;
③碱金属中还原性最强的是钾;
④碱金属阳离子,氧化性最强的是Li+;
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大;
⑥从Li到Cs,碱金属的密度越来越大,熔沸点越来越高.
| A、②③⑥ | B、②③④ |
| C、④⑤⑥ | D、①③⑤ |
考点:碱金属的性质
专题:金属概论与碱元素
分析:①钾的密度大于煤油,和空气中水蒸气、氧气、二氧化碳发生反应;
②碱金属常温下呈固态,是活泼金属和皮肤中水反应生成碱具有强腐蚀性,取用时不能直接用手拿;
③依据同主族性质递变分析;
④金属性越强,对应阳离子的氧化性越弱;
⑤同主族电子层数相同,随核电荷数增大而增大;
⑥从Li到Cs,碱金属的密度一般越来越大钾反常,熔沸点降低;
②碱金属常温下呈固态,是活泼金属和皮肤中水反应生成碱具有强腐蚀性,取用时不能直接用手拿;
③依据同主族性质递变分析;
④金属性越强,对应阳离子的氧化性越弱;
⑤同主族电子层数相同,随核电荷数增大而增大;
⑥从Li到Cs,碱金属的密度一般越来越大钾反常,熔沸点降低;
解答:
解:①钾的密度大于煤油,和空气中水蒸气、氧气、二氧化碳发生反应,少量K通常保存在煤油中,以隔绝与空气的接触,故①正确;
②碱金属是活泼金属和皮肤中水反应生成碱具有强腐蚀性,取用时不能直接用手拿,故②错误;
③依据同主族性质递变分析,碱金属中还原性最强的是钫,故③错误;
④金属性越强,对应阳离子的氧化性越弱,所以碱金属阳离子,氧化性最强的是Li+,故④正确;
⑤同主族电子层数相同,随核电荷数增大而增大,碱金属的原子半径和离子半径都随核电荷数的增大而增大,故⑤正确;
⑥从Li到Cs,碱金属的密度一般越来越大钾反常,从上到下熔沸点降低,故⑥错误;
故选A.
②碱金属是活泼金属和皮肤中水反应生成碱具有强腐蚀性,取用时不能直接用手拿,故②错误;
③依据同主族性质递变分析,碱金属中还原性最强的是钫,故③错误;
④金属性越强,对应阳离子的氧化性越弱,所以碱金属阳离子,氧化性最强的是Li+,故④正确;
⑤同主族电子层数相同,随核电荷数增大而增大,碱金属的原子半径和离子半径都随核电荷数的增大而增大,故⑤正确;
⑥从Li到Cs,碱金属的密度一般越来越大钾反常,从上到下熔沸点降低,故⑥错误;
故选A.
点评:本题考查了碱金属性质递变规律的分析判断,注意特征性质分析特殊物质性质的判断,掌握基础是关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质既属于钾盐又属于硫酸盐的是( )
| A、碳酸钾 | B、硫酸钠 |
| C、碳酸钠 | D、硫酸钾 |
下列说法正确的是( )
| A、元素铯的两种核素137Cs比133Cs多四个质子 |
| B、等质量的H2、D2、T2三种气体的电子数之比为2:3:6 |
| C、一种元素只能有一种质量数 |
| D、在氮原子中,质子数为7而中子数不一定为7 |
下列各组反应中,第一个反应放出的热量比第二个反应放出的热量多的是(g、l、s分别表示气体、液体、固体)( )
| A、2H2(g)+O2(g)=2H2O(1)2H2(g)+O2(g)=2H2O(g) | ||||
B、
| ||||
C、C(s)+
| ||||
| D、S(s)+O2(g)=SO2(g) S(g)+O2(g)=SO2(g) |
在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用( )
| A、NaCl |
| B、HC1 |
| C、NaOH |
| D、CuSO4 |
有机化学中取代反应范畴很广,下列反应不属于取代反应的是( )
A、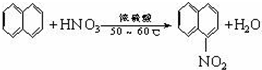 |
B、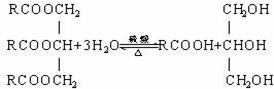 |
C、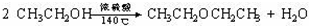 |
D、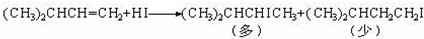 |
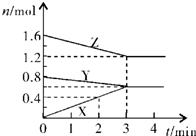
可逆反应2NO2
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
| △ |
| A、NO2、NO和O2三者共存 |
| B、单位时间内生成n molO2的同时生成2n mol NO |
| C、容器中颜色不再变化 |
| D、容器中NO2、NO、O2的物质的量浓度之比为2:2:1的状态 |
下列排列顺序错误的是( )
| A、酸性:H4SiO4<H3PO4<H2SO4<HClO4 |
| B、氢化物的稳定性:CH4<NH3<H2O<HF |
| C、碱性:KOH>Ca(OH)2>Mg(OH)2 |
| D、沸点:HI>HBr>HCl>HF |
 Ⅰ同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区分这些概念吗?下面列出了几组物质,请用物质的组号填写下表.
Ⅰ同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区分这些概念吗?下面列出了几组物质,请用物质的组号填写下表.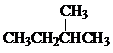 和
和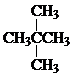
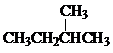 和
和