题目内容
12.能与Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液态)归为一类的物质是( )| A. | 液氨 | B. | HCl(气态) | C. | Fe(OH)3胶体 | D. | 固体五氧化二磷 |
分析 Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液态)都是溶于水或融化状态下能够导电的化合物,属于电解质,据此分析即可.
解答 解:Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液态)都是溶于水或融化状态下能够导电的化合物,属于电解质;液氨、固体五氧化二磷是非电解质;Fe(OH)3胶体是混合物,只有HCl(气态)是电解质,故选B.
点评 本题考查物质的分类的应用,仔细观察找出Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液态)的共性即可.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
7.在3个2L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)$?_{催化剂}^{高温、高压}$2NH3(g).按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
下列说法不正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2molNH2 |
| 达到平衡的时间/min | 5 | 8 | |
| 平衡时N2的浓度/mol.L-1 | c1 | 1.5 | |
| NH3的体积分数 | φ1 | φ2 | |
| 混合气体的密度/g.L-1 | ρ1 | ρ2 |
| A. | 容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol•L-1•min-1 | |
| B. | 2c1<1.5 | |
| C. | 在该温度下甲容器中反应的平衡常数K=$\frac{(2-2{c}_{1})^{2}}{{c}_{1}•(3{c}_{1}-1.5)^{3}}$ | |
| D. | 2ρ1=ρ2 |
17.下列有关化学知识或说法正确的是( )
| A. | 海洋中蕴含的元素有80多种,其中碘的储量可达8×1010t,所以碘被称为海洋元素 | |
| B. | 1774年瑞典科学家舍勒意外地发现一种黄绿色气体,并把它命名为氯气 | |
| C. | 19世纪科学家戴维首次用电解氯化钠溶液的方法制得金属钠 | |
| D. | 钠和钾的合金常温下是液体,可用于快中子反应堆的导热剂 |
4.根据如图海水综合利用的工业流程图,判断下列说法正确的是( )


| A. | 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 在过程②中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| C. | 从能量转换角度看氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 | |
| D. | 从第③步到第⑤步的目的是为了浓缩富集,提高Br2的浓度 |
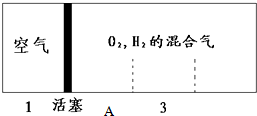 如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央A处,则原来H2、O2的体积比最接近于7:2 或4:5;此比例的H2和O2混合气体的平均摩尔质量为8.67g/mol或18.67g/mol.
如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央A处,则原来H2、O2的体积比最接近于7:2 或4:5;此比例的H2和O2混合气体的平均摩尔质量为8.67g/mol或18.67g/mol.
 +CO2+H2O→NaHCO3+
+CO2+H2O→NaHCO3+ .
.