题目内容
9.写出下列电子式:①NaOH ②N2
②N2 .
.
分析 氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氢氧根离子需要标出最外层电子;
氮气中存在3对共用电子对,氮原子最外层达到8个电子.
解答 解:氢氧化钠属于离子化合物,电子式中需要标出阴阳离子所带电荷,钠离子直接用离子符号表示,氢氧根离子需要标出最外层电子,氢氧化钠的电子式为: ,氮气中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气的电子式为
,氮气中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气的电子式为 ,
,
故答案为: ;
; .
.
点评 本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及正确的表示方法,明确离子化合物中阴离子需要标出最外层电子,阳离子直接用离子符号表示.

练习册系列答案
相关题目
20.分子式为 C5H8O2的有机物,能与NaHCO3溶液反应生成气体,则符合上述条件的同分异构体(不考虑立体异构)有( )
| A. | 8 种 | B. | 10 种 | C. | 11 种 | D. | 12 种 |
17.20世纪80年代后期人们逐渐认识到,NO是血压调节的主要因子,在心血管系统中起着重要的作用.下列关于NO的说法中,错误的是( )
| A. | NO是无色气体 | B. | NO是汽车尾气的有害成分之一 | ||
| C. | 可以用向上排空气法收集NO | D. | NO在一定条件下也可做氧化剂 |
14.下列各组物质中,互为同系物的是( )
| A. | 1H和2H | B. | O2和O3 | C. | CH4和C2H4 | D. | C3H8和C4H10 |
1.戊烷可能存在的同分异构体有( )
| A. | 3种 | B. | 2种 | C. | 4种 | D. | 5种 |
18.下列电离方程式或离子方程式书写正确的是( )
| A. | HF在水溶液中的电离方程式:HF=H++F- | |
| B. | 醋酸与氢氧化钠反应的离子方程式:H++OHˉ?H2O | |
| C. | NaHCO3在水溶液中的电离方程式:NaHCO3=Na++H++CO32ˉ | |
| D. | CuSO4在水溶液中水解的离子方程式:Cu2++2H2O?Cu (OH)2+2H+ |
19.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
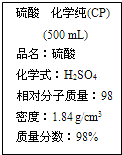

| A. | 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L | |
| B. | 1 mol Mg与足量该硫酸反应产生2 g氢气 | |
| C. | 配制250 mL 1.0 mol/L的稀硫酸需取该硫酸约13.6mL | |
| D. | 该硫酸溶液可作H2S的干燥剂 |