题目内容
20.为了证明化学反应有一定的限度,进行了如下探究活动:步骤1:取8mL0.1mol•L-1的KI溶液于试管,滴加0.1mol•L-1的FeCl3溶液5~6滴,振荡;
请写出步骤1中发生的离子反应方程式:2Fe3++2I-=2Fe2++I2
步骤2:在上述试管中加入2mLCCl4,充分振荡、静置;
步骤3:取上述步骤2静置分层后的上层水溶液少量于试管,滴加0.1mol•L-1的KSCN溶液5~6滴,振荡,未见溶液呈血红色.
探究的目的是通过检验Fe3+,来验证是否有Fe3+残留,从而证明化学反应有一定的限度.针对实验现象,同学们提出了下列两种猜想:
猜想一:KI溶液过量,Fe3+完全转化为Fe2+,溶液无Fe3+
猜想二:Fe3+大部分转化为Fe2+,使生成Fe(SCN)3浓度极小,肉眼无法观察其颜色
为了验证猜想,在查阅资料后,获得下列信息:
信息一:乙醚比水轻且微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大.
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高.
结合新信息,请你完成以下实验:各取少许步骤2静置分层后的上层水溶液于试管A、B中,请将相关的实验操作、预期现象和结论填入下表空白处:
| 实验操作 | 预期现象 | 结论 |
| 实验1:在试管A加入少量乙醚,充分振荡,静置 | 乙醚层呈红色 | “猜想一”不成立 |
| 实验2:取萃取后的上层清液滴加2-3滴 K4[Fe(CN)6]溶液 | 若产生蓝色沉淀 | 则“猜想二”成立 |
分析 (1)步骤1KI和FeCl3发生氧化还原反应生成I2、KCl和FeCl2;
(2)Fe(SCN)3在乙醚溶解度较大,显红色;
Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀
解答 解:(1)步骤1:活动(Ⅰ)KI和FeCl3发生氧化还原反应生成I2、KCl和FeCl2,发生反应:2KI+FeCl3=I2+2KCl+FeCl2,其离子反应为2Fe3++2I-=2Fe2++I2,
故答案为:2Fe3++2I-=2Fe2++I2;
(2)由信息一可得:往探究活动III溶液中加入乙醚,Fe(SCN)3在乙醚溶解度较大,充分振荡,乙醚层呈血红色,
由信息信息二可得:取萃取后的上层清液滴加2-3滴K4[Fe(CN)6]溶液,产生蓝色沉淀,
故答案为:
| 实验操作 | 现象 | 结论 |
| 乙醚层呈红色 | “猜想一”不成立 | |
| 取萃取后的上层清液滴加2-3滴 K4[Fe(CN)6]溶液 |
点评 本题主要考查了氧化还原反应、离子方程式的书写、反应的限度的探究,题目难度中等,抓住题干提供的信息是解答问题的关键,注意把握离子的检验方法,侧重于考查学生的分析能力和实验探究能力.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案
相关题目
10.在密闭容器中发生反应:aX(气)+bY(气)?cZ(气)+dW(气),反应达到平衡后,保持温度不变,将气体压缩到原来的$\frac{1}{2}$体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中正确的是( )
| A. | 平衡常数K增大 | B. | a+b<c+d | C. | X的转化率下降 | D. | Z的体积分数增加 |
8.某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为放热反应,中和反应都是放热反应,其实质是酸电离出的H+与碱电离出的OH-结合生成弱电解质水:H++OH-═H2O.
15.化学源于生活又用于生活,下列有关应用不正确的是( )
| A. | 用浸泡高锰酸钾溶液的硅土来吸收水果或花朵产生的乙烯以达到保鲜效果 | |
| B. | 淀粉、油脂、蛋白质都是天然高分子化合物 | |
| C. | 加热能杀死流感病毒是因为病毒的蛋白质受热变性 | |
| D. | 含硫化石燃料的大量燃烧是酸雨形成的主要原因之一 |
5.下列各组微粒互为同位素的是( )
| A. | 1H和2H | B. | 14C和14N | C. | 37Cl和37Cl - | D. | 56Fe2+和56Fe3+ |
12.下列各组物质中,一定互为同系物的是( )
| A. | C2H4和C8H8 | B. | 乙烷和己烷 | C. | 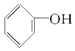 和 和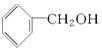 | D. | HCHO、CH3COOH |
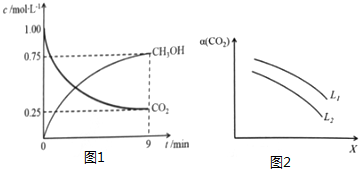 随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点..“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.(1)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
随着能源与环境问题越来越被人们关注,碳一化学(C1化学)成为研究的热点..“碳一化学”即以单质碳及CO、CO2、CH4、CH3OH等含一个碳原子的物质为原料合成工业产品的化学与工艺.(1)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如: