题目内容
20.下列组合中,属于含有极性键的非极性分子的是( )| A. | C2H4、C2H2、CO2 | B. | CH4、CHCl3、CO2 | C. | Cl2、H2、N2 | D. | NH3、H2O、CO2 |
分析 同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性键,由极性键构成的分子,结构对称,正负电荷的中心重合,则为非极性分子.
解答 解:A.C2H4中有C、H元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子;C2H2中有C、H元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子;CO2中有C、O元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子,故A正确;
B.CH4 中含有极性键,为正四面体结构,结构对称,分子中正负电荷重心重叠,为非极性分子;CHCl3有C、H和C、O元素之间形成极性键;但结构不对称,正负电荷的中心不重合,属于极性分子;CO2中有C、O元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子,故B错误;
C.Cl2中只有Cl-Cl非极性键,属于非极性分子;H2中只有H-H非极性键,属于非极性分子;N2中只有N-N非极性键,属于非极性分子,故C错误;
D.NH3中有N、H元素形成的极性键,但结构不对称,属于极性分子;H2O中H、O元素形成的极性键,但结构不对称,属于极性分子;CO2中有C、O元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子,故D错误;
故选A.
点评 本题考查化学键及分子的极性,明确化学键判断的方法及分子极性的判断方法是解答本题的关键,应熟悉常见分子的构型,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
10.下列说法正确的是( )
| A. | AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 | |
| B. | 配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 | |
| C. | 用加热的方法可除去KNO3溶液中混有的FeCl3 | |
| D. | Na2CO3溶液加水稀释后,恢复至室温,pH和Kw均减小 |
11.甲溶液的pH=2,乙溶液的pH=4,甲溶液与乙溶液的c(H+)之比是( )
| A. | 1:2 | B. | 2:1 | C. | 1:100 | D. | 100:1 |
8.最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”-全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划.有关全氟丙烷的说法正确的是( )
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的电子式为: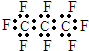 | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 一个全氟丙烷分子中有10个共用电子对 |
15.有两个无标签的试剂瓶,分别盛有固体K2CO3、NaHCO3,有四位同学为鉴别它们采用了以下不同方法,其中不可行的是( )
| A. | 分别将它们配制成溶液,再加入澄清石灰水,观察是否有沉淀产生 | |
| B. | 分别将它们配制成溶液,再进行焰色反应,观察火焰颜色 | |
| C. | 分别将它们配制成溶液,再加入BaCl2溶液,观察是否有沉淀产生 | |
| D. | 分别加热,再用澄清石灰水检验是否有气体产生 |
5.下列除去杂质的方法正确的是( )
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | NaHC03固体 | Na2C03固体 | / | 加热 |
| B | Al2O3 | Fe2O3 | 盐酸 | 过滤 |
| C | KBr溶液 | Br2 | KOH溶液 | 分液 |
| D | Cl2 | HCl | 饱和食盐水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
9.生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应).
【相关资料】
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在.
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计.
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化.
【实验过程】
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(l)请完成以下实验设计表(表中不要留空格)
实验测得含氰废水中的总氰浓度(以CN-表示)随时间变化关系如图所示.

(2)实验①中20~60min时间段反应速率:υ(CN-)=0.0175mol•L-1•min-1.
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用(或初始pH增大,[Fe(CN)6]3-较中性和酸性条件下更稳定,难以氧化)(填一点即可).在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO3-,同时放出NH3,试写出该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成下表中内容.(己知:废水中的CN-浓度可用离子色谱仪测定)
【相关资料】
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在.
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计.
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化.
【实验过程】
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(l)请完成以下实验设计表(表中不要留空格)
| 实验 序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
| ① | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
| ② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| ③ | 双氧水的浓度对破氰反应速率的影响 | 7 | 60 | 10 | 20 | 10 |

(2)实验①中20~60min时间段反应速率:υ(CN-)=0.0175mol•L-1•min-1.
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用(或初始pH增大,[Fe(CN)6]3-较中性和酸性条件下更稳定,难以氧化)(填一点即可).在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO3-,同时放出NH3,试写出该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成下表中内容.(己知:废水中的CN-浓度可用离子色谱仪测定)
| 实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |
10.下列物质中,属于电解质的是( )
| A. | NaOH | B. | CH3CH2OH(酒精) | C. | 蔗糖 | D. | CO2 |