题目内容
铁是一种应用广泛的金属.下列有关铁的说法错误的是( )
| A、铁与盐酸反应生成氯化铁与氢气 |
| B、常温下,铁在浓硫酸中会发生钝化 |
| C、铁在氧气中燃烧生成四氧化三铁 |
| D、铁是一种银白色金属 |
考点:铁的化学性质
专题:元素及其化合物
分析:A.反应生成氯化亚铁和氢气;
B.浓硫酸具有强氧化性;
C.燃烧生成四氧化三铁;
D.纯铁为银白色金属.
B.浓硫酸具有强氧化性;
C.燃烧生成四氧化三铁;
D.纯铁为银白色金属.
解答:
解:A.铁与盐酸反应生成氯化亚铁和氢气,与强氧化剂反应生成铁离子,故A错误;
B.浓硫酸具有强氧化性,则常温下铁在浓硫酸中钝化生成致密的氧化物薄膜阻止反应的进一步发生,故B正确;
C.铁在氧气中燃烧生成四氧化三铁,为黑色固体,故C正确;
D.纯铁为银白色金属,为金属的通性,故D正确;
故选A.
B.浓硫酸具有强氧化性,则常温下铁在浓硫酸中钝化生成致密的氧化物薄膜阻止反应的进一步发生,故B正确;
C.铁在氧气中燃烧生成四氧化三铁,为黑色固体,故C正确;
D.纯铁为银白色金属,为金属的通性,故D正确;
故选A.
点评:本题考查铁的化学性质,注意Fe与不同氧化剂反应的产物,明确氧化性的强弱是解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
下列说法错误的是( )
| A、乙醇和乙酸都是常用调味品的主要成分 |
| B、乙醇和乙酸都能发生加成反应 |
| C、乙醇和乙酸都能发生氧化反应 |
| D、乙醇和乙酸之间能发生酯化反应 |
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰.电池总反应为Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、电池正极反应式为2MnO2+2H2O+2e-═2MnO(OH)+2OH- |
| B、电池工作时,电子通过外电路从正极流向负极 |
| C、当0.1 mol Zn完全溶解时,流经电解液的电子个数为1.204×1023 |
| D、该电池反应中二氧化锰起催化作用 |
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
| A、b、a、e、d、c |
| B、e、d、a、b、c |
| C、a、b、d、c、e |
| D、c、d、e、a、b |
用NA代表阿伏伽德罗常数的值.下列叙述正确的是( )
| A、1mol乙烷分子中含有8NA个共价键 |
| B、0.05mol熔融的KHSO4中含有阳离子的数目为0.05 NA |
| C、标准状况下,22.4L甲醇的分子数为NA |
| D、1mol/L的氯化铵溶液含氮原子数为 NA |
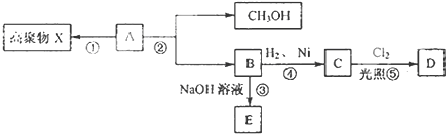
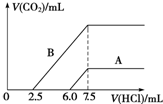 含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.
含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.