题目内容
用NA代表阿伏伽德罗常数的值.下列叙述正确的是( )
| A、1mol乙烷分子中含有8NA个共价键 |
| B、0.05mol熔融的KHSO4中含有阳离子的数目为0.05 NA |
| C、标准状况下,22.4L甲醇的分子数为NA |
| D、1mol/L的氯化铵溶液含氮原子数为 NA |
考点:阿伏加德罗常数
专题:
分析:A、由乙烷分子中有六个碳氢键、一个碳碳键;
B、熔融硫酸氢钾中的阳离子为钠离子;
C、标况下,甲醇为液态;
D、溶液体积不明确.
B、熔融硫酸氢钾中的阳离子为钠离子;
C、标况下,甲醇为液态;
D、溶液体积不明确.
解答:
解:A、由乙烷分子中有六个碳氢键、一个碳碳键,则1mol乙烷分子含有7NA个共价键,故A错误;
B、0.05mol熔融硫酸氢钾中含有0.05mol阳离子钠离子,含有阳离子的数目为0.05NA,故B正确;
C、标况下,甲醇为液态,故C错误;
D、溶液体积不明确,故无法计算溶液中氮原子的个数,故D错误.
故选B.
B、0.05mol熔融硫酸氢钾中含有0.05mol阳离子钠离子,含有阳离子的数目为0.05NA,故B正确;
C、标况下,甲醇为液态,故C错误;
D、溶液体积不明确,故无法计算溶液中氮原子的个数,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
铁是一种应用广泛的金属.下列有关铁的说法错误的是( )
| A、铁与盐酸反应生成氯化铁与氢气 |
| B、常温下,铁在浓硫酸中会发生钝化 |
| C、铁在氧气中燃烧生成四氧化三铁 |
| D、铁是一种银白色金属 |
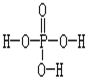 磷酸的结构式如图所示,磷酸分子与磷酸分子的羟基之间可以脱去水.三个磷酸分子可以脱去两个水分子生成三聚磷酸.含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )
磷酸的结构式如图所示,磷酸分子与磷酸分子的羟基之间可以脱去水.三个磷酸分子可以脱去两个水分子生成三聚磷酸.含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )| A、Na5P3O1212mol |
| B、Na3H2P3O10 9mol |
| C、Na5P3O109mol |
| D、Na2H3P3O10 12mol |
赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu2O+Cu2S
6Cu+SO2↑.对于该反应,下列说法正确的是( )
| ||
| A、该反应的氧化剂只有Cu2O |
| B、还原产物与氧化产物的物质的量之比为1:6 |
| C、Cu2S在反应中既是氧化剂,又是还原剂 |
| D、Cu既是氧化产物又是还原产物 |
下列离子方程式书写正确的是( )
| A、硫酸铝溶液中滴加过量浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、乙酸钠溶液显碱性原因:CH3COO-+H2O=CH3COOH+OH- |
| C、氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO32-+H2O |
| D、漂白粉放置在空气中变质:ClO-+CO2+H2O=HClO+HCO3- |
取一份矿石试样进行实验,首先将其溶于过量的盐酸,过滤后,向所得的沉淀X和溶液Y中分别加入NaOH溶液至过量(该矿石可看作由MgO、A12O3、SiO2、Fe2O3等矿物组成).则下列叙述错误的是( )
| A、溶液Y中加入过量的NaOH溶液后过滤,滤液和沉淀中各含两种金属元素 |
| B、该矿石成分中能溶于盐酸的都是碱性氧化物,不溶的是酸性氧化物 |
| C、溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+ |
| D、沉淀X的成分是SiO2 |
 锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.
锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.