题目内容
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰.电池总反应为Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、电池正极反应式为2MnO2+2H2O+2e-═2MnO(OH)+2OH- |
| B、电池工作时,电子通过外电路从正极流向负极 |
| C、当0.1 mol Zn完全溶解时,流经电解液的电子个数为1.204×1023 |
| D、该电池反应中二氧化锰起催化作用 |
考点:化学电源新型电池
专题:
分析:根据电池反应式知,Zn失电子发生氧化反应而作负极,负极反应式为Zn-2e-+2OH-═ZnO+H2O,MnO2被还原,为原电池的正极,电极反应为2MnO2+2H2O+2e-═2MnO(OH)+2OH-.
解答:
解:A.根据电池反应式知,正极上MnO2被还原,电极反应为2MnO2+2H2O+2e-═2MnO(OH)+2OH-,故A正确;
B.放电时,电子从负极沿外电路流向正极,故B错误;
C.电子不进入电解质溶液,电解质溶液中阴阳离子定向移动形成电流,故C错误;
D.该反应中正极上二氧化锰发生还原反应,二氧化锰参加反应,所以不是催化剂,故D错误;
故选A.
B.放电时,电子从负极沿外电路流向正极,故B错误;
C.电子不进入电解质溶液,电解质溶液中阴阳离子定向移动形成电流,故C错误;
D.该反应中正极上二氧化锰发生还原反应,二氧化锰参加反应,所以不是催化剂,故D错误;
故选A.
点评:本题考查化学电源新型电池,会根据元素化合价变化确定正负极,会正确书写电极反应式,易错选项是C,注意电子不进入电解质溶液.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列小实验不能制得溶液的是( )
A、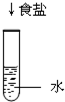 |
B、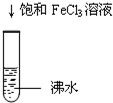 |
C、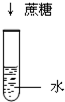 |
D、 |
从我国西部开采的天然气,通过西气东输工程供给江苏.天然气的主要成分是( )
| A、甲烷 | B、氢气 |
| C、一氧化碳 | D、乙烯 |
铁是一种应用广泛的金属.下列有关铁的说法错误的是( )
| A、铁与盐酸反应生成氯化铁与氢气 |
| B、常温下,铁在浓硫酸中会发生钝化 |
| C、铁在氧气中燃烧生成四氧化三铁 |
| D、铁是一种银白色金属 |
在25℃、101KPa下,1g甲醇燃烧生成CO2和液态水时放热22.68KJ,下列热化学方程正确的是( )
A、CH3OH(l)+
| ||
| B、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452KJ/mol | ||
C、CH3OH(l)+
| ||
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1452KJ/mol |
下列说法正确的是( )
| A、物质发生化学变化都伴随着能量变化 |
| B、伴有能量变化的物质变化都是化学变化 |
| C、在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定相等 |
| D、在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |

 锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.
锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.