题目内容
下列说法正确的是( )
| A、弱碱溶于水后能促进水的电离 |
| B、盐溶于水后一定能促进水的电离 |
| C、任何条件下,只要pH>7,溶液就一定显碱性 |
| D、任何条件下,只要c(H+)>c(OH-),溶液就一定显酸性 |
考点:水的电离
专题:
分析:A、根据水的电离方程式H2O?H++OH-,酸、碱溶液都抑制了水的电离;
B、只有水解的盐才能促进水的电离;
C、溶液的酸碱性取决于溶液中c(OH-)、c(H+)的相对大小;
D、溶液的酸碱性与c(OH-)、c(H+)的相对大小有关.
B、只有水解的盐才能促进水的电离;
C、溶液的酸碱性取决于溶液中c(OH-)、c(H+)的相对大小;
D、溶液的酸碱性与c(OH-)、c(H+)的相对大小有关.
解答:
解:A、酸溶液中的氢离子、碱溶液中的氢氧根离子,都会抑制水的电离,导致水的电离程度减小,故A错误;
B、只有能水解的盐才能促进水的电离,故B错误;
C、溶液的酸碱性与溶液中的c(OH-)、c(H+)有关,水的离子积受温度影响,pH>7,溶液中的c(OH-)、c(H+)大小关系不能确定,无法判断溶液的酸碱性,故C错误;
D、溶液的酸碱性取决于溶液中c(OH-)、c(H+)的相对大小,如果c(OH-)<c(H+),则溶液呈酸性,如果c(OH-)=c(H+)则溶液呈中性,溶液c(OH-)>c(H+),则溶液呈碱性,故D正确;
故选D.
B、只有能水解的盐才能促进水的电离,故B错误;
C、溶液的酸碱性与溶液中的c(OH-)、c(H+)有关,水的离子积受温度影响,pH>7,溶液中的c(OH-)、c(H+)大小关系不能确定,无法判断溶液的酸碱性,故C错误;
D、溶液的酸碱性取决于溶液中c(OH-)、c(H+)的相对大小,如果c(OH-)<c(H+),则溶液呈酸性,如果c(OH-)=c(H+)则溶液呈中性,溶液c(OH-)>c(H+),则溶液呈碱性,故D正确;
故选D.
点评:本题考查了水的电离及溶液的酸碱性的判断,注意溶液的酸碱性取决于溶液中c(OH-)、c(H+)的相对大小,本题难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
化学与社会、生产、生活紧切相关.下列说法正确的是( )
| A、棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 |
| B、石油干馏可得到石油气、汽油、煤油、柴油等 |
| C、从海水中提取物质都必须通过化学反应才能实现 |
| D、纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污 |
在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是( )
| A、加MgCl2 |
| B、加H2O |
| C、加NaOH |
| D、加HCl |
在相同温度下用惰性电极电解下列物质的水溶液,一段时间后溶液酸性增强或碱性减弱的是( )
| A、HCl |
| B、NaOH |
| C、Na2SO4 |
| D、CuSO4 |
已知工业合成氨:2N2(g)+6H2(g)?4NH3(g)△H=-184.8kJ/mol.一定条件下,现有容积相同且恒容的密闭容器甲与乙:①向甲中通入1mol N2和3mol H2,达到平衡时放出热量Q1 kJ;②向乙中通入0.5mol N2和1.5mol H2,达到平衡时放出热量Q2kJ.则下列关系式正确的是( )
| A、92.4=Q1<2Q2 |
| B、92.4>Ql>2Q2 |
| C、Q1=2Q2=92.4 |
| D、Q1=2Q2<92.4 |
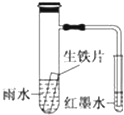 双鸭山一中某化学兴趣小组研究酸雨对生铁腐蚀情况的实验如下:图示小试管内为红色的墨水,具支试管中为pH=4.5放置一段时间的雨水和生铁.实验观察到:初期导管内液面下降,后来导管内液面回升,略高于小试管内液面.下列说法正确的是( )
双鸭山一中某化学兴趣小组研究酸雨对生铁腐蚀情况的实验如下:图示小试管内为红色的墨水,具支试管中为pH=4.5放置一段时间的雨水和生铁.实验观察到:初期导管内液面下降,后来导管内液面回升,略高于小试管内液面.下列说法正确的是( )| A、生铁片中的碳是原电池的负极,发生还原反应 |
| B、雨水酸性较强,生铁片始终发生析氢腐蚀 |
| C、墨水回升时,碳电极反应式为O2+2H2O+4e-═4OH- |
| D、具支试管中溶液酸性增强 |
某反应的离子方程式为Ca2++CO32-═CaCO3↓,对该反应的下列说法不正确的是( )
| A、该反应可能是化合反应,也可能是氧化还原反应 |
| B、该反应一定是复分解反应,且属于非氧化还原反应 |
| C、该反应可能是CaCl2+Na2CO3═CaCO3↓+2NaCl |
| D、该反应可能是Ca(OH)2+K2CO3═CaCO3↓+2KOH |
X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期.X原子的外围电子排布式为nSnnPn+2.Z原子的核电荷数是最外层电子数的三倍.下列说法正确的是( )
| A、原子序数由大到小的顺序为Z<Y<X |
| B、Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C、3种元素的气态氢化物中Z的气态氢化物最稳定 |
| D、原子半径由大到小的顺序为Z>Y>X |
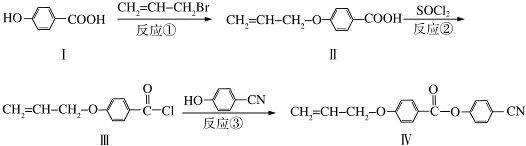
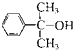 也可与III发生类似反应③的反应生成有机物V,V的结构简式是
也可与III发生类似反应③的反应生成有机物V,V的结构简式是