题目内容
如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面图.下列说法正确的是( )
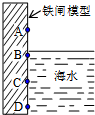

| A、该电化腐蚀为析氢腐蚀 |
| B、图中生成铁锈最多的是C区域 |
| C、A区域比B区域更易腐蚀 |
| D、铁闸中的负极的电极反应:Fe-2e-=Fe2+ |
考点:金属的电化学腐蚀与防护
专题:
分析:A.海水溶液为弱酸性,发生吸氧腐蚀;
B.在B处最易形成原电池;
C.根据吸氧腐蚀的发生条件分析;
D.Fe作负极失电子生成亚铁离子.
图中A发生化学腐蚀,B发生电化学腐蚀,C已经腐蚀后有氧化层,D在金属内部.
B.在B处最易形成原电池;
C.根据吸氧腐蚀的发生条件分析;
D.Fe作负极失电子生成亚铁离子.
图中A发生化学腐蚀,B发生电化学腐蚀,C已经腐蚀后有氧化层,D在金属内部.
解答:
解:A.海水溶液为弱酸性,发生吸氧腐蚀,在酸性较强的条件下才发生析氢腐蚀,故A错误;
B.在B处,海水与氧气接触,与Fe最易形成原电池,发生的吸氧腐蚀的程度最大,生成铁锈最多,故B错误;
C.在B处,海水与氧气接触,与Fe最易形成原电池,所以B区域比A区域更易腐蚀,故C错误;
D.Fe作负极失电子生成亚铁离子,则负极的电极反应:Fe-2e-=Fe2+,故D正确.
故选D.
B.在B处,海水与氧气接触,与Fe最易形成原电池,发生的吸氧腐蚀的程度最大,生成铁锈最多,故B错误;
C.在B处,海水与氧气接触,与Fe最易形成原电池,所以B区域比A区域更易腐蚀,故C错误;
D.Fe作负极失电子生成亚铁离子,则负极的电极反应:Fe-2e-=Fe2+,故D正确.
故选D.
点评:本题考查了金属的电化学腐蚀,明确吸氧腐蚀发生的条件是解题的关键,题目难度不大.

练习册系列答案
相关题目
下列各组中的两种物质作用,反应条件或者反应物用量改变,不会引起产物种类改变的是( )
| A、Na和O2 |
| B、NaOH和CO2 |
| C、Fe和Cl2 |
| D、AlCl3和NaOH |
能确定为丙烯的化学用语是( )
A、 |
| B、C3H6 |
C、 |
| D、CH2=CH-CH3 |
已知工业合成氨:2N2(g)+6H2(g)?4NH3(g)△H=-184.8kJ/mol.一定条件下,现有容积相同且恒容的密闭容器甲与乙:①向甲中通入1mol N2和3mol H2,达到平衡时放出热量Q1 kJ;②向乙中通入0.5mol N2和1.5mol H2,达到平衡时放出热量Q2kJ.则下列关系式正确的是( )
| A、92.4=Q1<2Q2 |
| B、92.4>Ql>2Q2 |
| C、Q1=2Q2=92.4 |
| D、Q1=2Q2<92.4 |
下列状态的物质,既属于电解质又能导龟的是( )
| A、氯化镁晶体 |
| B、氯化钠溶液 |
| C、液态氯化氢 |
| D、熔融氢氧化钾 |
某反应的离子方程式为Ca2++CO32-═CaCO3↓,对该反应的下列说法不正确的是( )
| A、该反应可能是化合反应,也可能是氧化还原反应 |
| B、该反应一定是复分解反应,且属于非氧化还原反应 |
| C、该反应可能是CaCl2+Na2CO3═CaCO3↓+2NaCl |
| D、该反应可能是Ca(OH)2+K2CO3═CaCO3↓+2KOH |
 E~N等元素在周期表中的相对位置如下表.E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是( )
E~N等元素在周期表中的相对位置如下表.E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是( )| A、K的氢化物水溶液显碱性 |
| B、F的单质与氧气反应只生成一种氧化物 |
| C、H与N的原子核外电子数相差14 |
| D、最高价氧化物的水化物酸性:K>L>M |
常温下,某弱酸的酸式盐NaHA溶液中,c(OH-)<c(A2-),下列有关溶液的说法中正确的是( )
| A、溶液的PH>7 |
| B、溶液中c(Na+)=2c(A2-)+c(HA)+c(H2A) |
| C、加水稀释,c(A2-)/c(HA-)减小 |
| D、加入NaOH固体,可使离子浓度满足:c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) |