题目内容
17.关于1s、2s、3s、4s原子轨道的说法,正确的是( )| A. | 电子只能在电子云轮廓图中运动 | |
| B. | 能层不同,电子云轮廓图形状不相同 | |
| C. | 轨道数目相同,电子云轮廓图形状、大小完全相同 | |
| D. | 能层不同,能级相同,电子云轮廓图形状相同 |
分析 电子云表示电子出现的几率,即表示电子在核外单位体积的空间出现的机会多少;能级相同,电子云轨道形状相同,S能级上电子的电子云为球形,与能层数无关.
解答 解:A.电子云表示电子出现的几率,电子在电子云轮廓图中出现的机会多,但也会出现在轮廓图外,但机会较少,故A错误;
B.能层不同,但能级相同的轨道,其电子云轮廓图形状相同,故B错误;
C.轨道数目相同,电子云轮廓图形状相同,大小不同,故C错误;
D.能层不同,电子云形状可能相同,如1s、2s能级上电子的电子云形状相同,均为球形,故D正确;
故选D.
点评 本题考查了电子云的有关知识,题目难度不大,明确电子云的含义是解本题关键,知道电子云形状相同的电子其能层不一定相同,为易错点.

练习册系列答案
相关题目
7.下列反应中不属于可逆反应的是( )
| A. | 氮气和氢气的化合 | B. | 氯气溶于水 | ||
| C. | 氨气溶于水 | D. | 水的电解 |
12.在常温下,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 0.1 mol•L-1 pH=7.82 的 NH4HCO3 溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 0.1 mol•L-1 Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) | |
| C. | 浓度均为 0.1 mol•L-1的NH3•H2O 溶液和 NH4Cl 溶液等体积混合:c(NH4+)+c(H+)>c(NH3•H2O)+c(OH-) | |
| D. | 0.1 mol•L-1 Na2S 溶液与 0.1 mol•L-1 NaHS 溶液等体积混合:2c(Na+)-3c(S2-)=3c(HS-)+3c(H2S) |
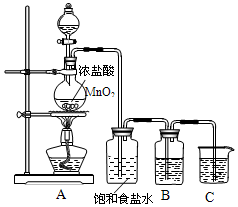 实验室制取氯气的装置如图:
实验室制取氯气的装置如图: