题目内容
13.下列实验能获得成功的是( )| A. | 苯、溴水、铁粉混合制成溴苯 | |
| B. | 甲烷与氯气光照制得纯净的一氯甲烷 | |
| C. | 乙烯通入溴的四氯化碳溶液得到1,2-二溴乙烷 | |
| D. | 用高锰酸钾溶液除去乙烷中的乙烯杂质 |
分析 A.苯和液溴在溴化铁作催化剂条件下发生取代反应生成溴苯;
B.甲烷和氯气在光照条件下发生取代反应生成多种氯代烃;
C.乙烯和溴发生加成反应;
D.乙烯能被酸性高锰酸钾溶液氧化生成二氧化碳.
解答 解:A.苯和液溴在溴化铁作催化剂条件下发生取代反应生成溴苯,苯和溴水不反应,故A错误;
B.甲烷和氯气在光照条件下发生取代反应生成多种氯代烃,所以得不到纯净物,故B错误;
C.乙烯中还有碳碳双键,性质较活泼,乙烯和溴发生加成反应生成1,2-二溴乙烷,故C正确;
D.乙烯能被酸性高锰酸钾溶液氧化生成二氧化碳,应该用溴水除去乙烷中的乙烯,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及物质制备、除杂等知识点,明确实验原理及物质性质差异性是解本题关键,易错选项是D.

练习册系列答案
相关题目
4.下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白
(1)这11种元素中化学性质最不活泼的是Ar,金属性最强的是K.(写元素符号)
(2)第三周期元素中,原子半径最大的元素是(稀有气体元素除外)Na,离子半径最小的是Al,单质氧化性最强的元素是Cl.(写元素符号)
(3)J的简单离子的结构示意图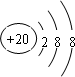 .
.
(4)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)KOH>NaOH>Mg(OH)2>Al(OH)3.
(5)比较G、H两元素的最高价氧化物对应水化物的酸性HClO4>H2SO4.比较C、G两元素的气态氢化物稳定性HCl>H2S.(写化学式)
(6)C和D的单质在点燃条件下生成化合物的电子式为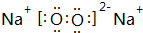 ,它属于离子(离子或共价)化合物.
,它属于离子(离子或共价)化合物.
(7)用电子式表示A和G所形成的简单化合物的形成过程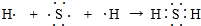 .
.
| 族 周期 | IA | IIA | IIIA | IV A | V A | VI A | VII A | O |
| 一 | A | |||||||
| 二 | B | C | ||||||
| 三 | D | E | F | G | H | I | ||
| 四 | K | J | ||||||
(2)第三周期元素中,原子半径最大的元素是(稀有气体元素除外)Na,离子半径最小的是Al,单质氧化性最强的元素是Cl.(写元素符号)
(3)J的简单离子的结构示意图
 .
.(4)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)KOH>NaOH>Mg(OH)2>Al(OH)3.
(5)比较G、H两元素的最高价氧化物对应水化物的酸性HClO4>H2SO4.比较C、G两元素的气态氢化物稳定性HCl>H2S.(写化学式)
(6)C和D的单质在点燃条件下生成化合物的电子式为
 ,它属于离子(离子或共价)化合物.
,它属于离子(离子或共价)化合物.(7)用电子式表示A和G所形成的简单化合物的形成过程
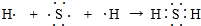 .
.
8.下列反应可用于设计原电池的是( )
| A. | CO2+2H2O→CH4+2O2 | B. | NaOH+HCl=NaCl+H2O | ||
| C. | Cu+2HCl=Cu Cl2+H2↑ | D. | 4Al+3O2+6H2O=4Al(OH)3 |
18.下列有关物质的性质或应用的说法正确的是( )
| A. | 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于侧链与苯环的相互影响,使侧链和苯环均易被氧化 | |
| B. | 等质量的乙烷、乙烯、乙炔在氧气中完全燃烧,乙烷消耗的氧气最多 | |
| C. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 | |
| D. | 可向溴乙烷中加入硝酸银溶液检验溴元素 |
5.下列离子方程式书写正确的是( )
| A. | 硅与氢氧化钾溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ | |
| B. | Al(OH)3溶于稀硝酸:OH-+H+═H2O | |
| C. | 往氨水中加入少量AlCl3溶液:Al3++4OH-═[Al(OH)4]- | |
| D. | 把水玻璃滴入盐酸中:SiO32-+2H+═H2SiO3 |
2.向某密闭容器中加入0.3mol A、0.1mol C和一定量B的混合气体,在一定条件下发生反应,各物质的浓度随时间变化如图甲所示(t0~t1阶段的c(B)变化未画出),图乙为t2时刻改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段各改变一种不同的反应条件.下列说法中正确的是( )
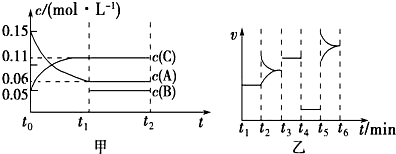

| A. | 若t1=15 s,t0~t1阶段B的平均反应速率为0.004 mol•L-1•s-1 | |
| B. | t4~t5阶段改变的条件是减小压强 | |
| C. | 该容器的容积为2 L,B的起始物质的量为0.02 mol | |
| D. | t5~t6阶段,容器内A的物质的量减少了0.06 mol,容器与外界的热交换为a kJ,则该反应的热化学方程式为3A(g)?B(g)+2C(g)△H=-50a kJ•mol-1 |
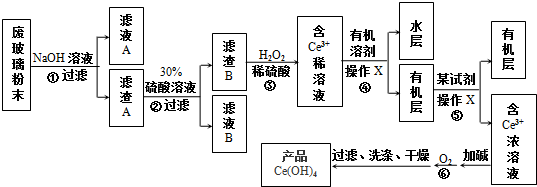
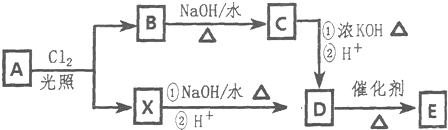
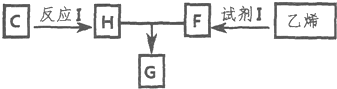
 (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).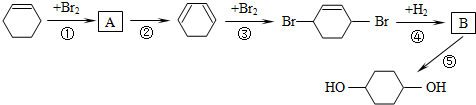
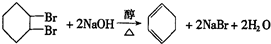
 .
.
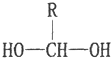 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$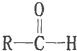

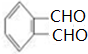 +4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$
+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$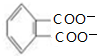 +2NH4++4Ag+6NH3+2H2O
+2NH4++4Ag+6NH3+2H2O .
. .
.
 .
.