题目内容
16.回答下题;(1)下列原子:${\;}_{6}^{14}$C、${\;}_{7}^{14}$N、${\;}_{11}^{23}$Na、${\;}_{1}^{3}$H、${\;}_{92}^{235}$U、${\;}_{19}^{40}$K、${\;}_{92}^{238}$U中共有6种元素,7种核素,23592U和23892U互为同位素.
(2)阴离子的中子数为N:AXn-共有x个电子,则N=A-x+n..
(3)书写电子式 HClO
 NaCl
NaCl .
.
分析 (1)元素就是具有相同的核电荷数(即核内质子数)的一类原子的总称;
核素是指具有一定数目质子和一定数目中子的一种原子;
具有相同质子数,不同中子数同一元素的不同核素互为同位素.
(2)阴离子中:质子数=核外电子数-所带电荷数,又根据质量数=质子数+中子数可以计算中子数.
(3)要求掌握常见物质电子式的书写方法,见解析.
解答 解:(1)元素的种类由质子数决定,质子数不同,元素的种类就不同,以上共有6种元素;
具有一定数目质子和一定数目中子的一种原子就是一种核素,因此共有7种核素;
质子数相同,中子数不同,23592U和23892U都是铀元素的不同核素,互为同位素.
故答案为:6;7;23592U和23892U;
(2)在阴离子中:质子数=核外电子数-所带电荷数,即核电荷数=质子数=x-n,又根据质量数=质子数+中子数,即中子数=质量数-质子数=A-(x-n).
故答案为:A-x+n.
(3)HClO中O原子分别与H、Cl原子形成共用电子对,电子式为 ;
;
NaCl为离子化合物,钠离子直接用离子符号表示,氯离子需要标出最外层8个电子,并用其“[]”括起来,右上角表明电荷,电子式为
故答案为: ;
;
点评 本题考查了元素、同位素概念和原子结构、电子式的书写方法,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列关于液氯和氯水的叙述中正确的是( )
| A. | 液氯是纯净物,而氯水是混合物 | B. | 液氯有酸性,氯水有漂白性 | ||
| C. | 液氯较氯水的漂白作用更强 | D. | 液氯无色,氯水呈黄绿色 |
11.下列说法正确的是( )
| A. | NH3可以用来做喷泉实验是因为其有特殊气味 | |
| B. | 工业上用氨和二氧化碳合成尿素属于氮的固定 | |
| C. | 液氨作制冷剂原因是其气化时大量吸收周围的热量 | |
| D. | NH3能使无色酚酞溶液变红 |
1.木糖醇是一种新型的甜味剂,溶解性好,防龋齿,适合糖尿病患者的需要.其结构简式为:HOCH2(CHOH)3CH2OH.下列有关木糖醇的叙述中不正确的是( )
| A. | 木糖醇是一种单糖,不能发生水解反应 | |
| B. | 木糖醇不属于糖类,它是多元醇 | |
| C. | 木糖醇易溶解于水,能发生酯化反应 | |
| D. | 1mol木糖醇与足量钠反应最多可产生2.5molH2 |
8.现拟分离乙酸乙酯、乙酸、乙醇的混合物,图是分离操作流程图.
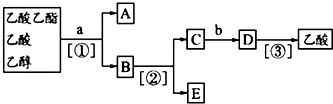
上述实验过程中涉及的三次分离操作分别是( )

上述实验过程中涉及的三次分离操作分别是( )
| A. | ①蒸馏 ②过滤 ③分液 | B. | ①分液 ②蒸馏 ③蒸馏 | ||
| C. | ①蒸馏 ②分液 ③分液 | D. | ①分液 ②蒸馏 ③结晶 过滤 |
5.由-H、-CH3、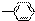 、-OH、-COOH五种原子或原子团中的任意两种,两两组合形成的物质中,溶液显酸性的物质有( )
、-OH、-COOH五种原子或原子团中的任意两种,两两组合形成的物质中,溶液显酸性的物质有( )
 、-OH、-COOH五种原子或原子团中的任意两种,两两组合形成的物质中,溶液显酸性的物质有( )
、-OH、-COOH五种原子或原子团中的任意两种,两两组合形成的物质中,溶液显酸性的物质有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
6.下列说法正确的是( )
| A. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| B. | HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | |
| C. | 元素周期律是元素原子核外电子排布周期性变化的结果 | |
| D. | 形成离子键的阴、阳离子间只存在静电吸引力 |
