题目内容
19.25℃时,将0.01mol CH3COONa 和0.002molHCl溶于水,形成1L混合溶液:(1)溶液中共有7种不同的粒子(指分子和离子).
(2)在这些粒子中,浓度为0.01mol/L的是Na+,浓度为0.002mol/L的是Cl-.
(3)在上述溶液中,物料守恒表达式n(CH3COOH)+n(CH3COO-)=0.01mol.
分析 (1)0.01molCH3COONa和0.002molHCl溶于水得到0.008molCH3COONa、0.002molCH3COOH、0.002molNaCl,CH3COONa、NaCl为强电解质,CH3COOH为弱电解质;
(2)根据钠离子、氯离子的物质的量来分析;
(3)根据物料守恒来分析.
解答 解:(1)0.01molCH3COONa和0.002molHCl溶于水得到0.008molCH3COONa、0.002molCH3COOH、0.002molNaCl,CH3COONa、NaCl为强电解质,CH3COOH为弱电解质,则溶液中存在的离子为:Na+、H+、Cl-、OH-、CH3COO-,存在的分子为:H2O、CH3COOH,即共有7种不同的微粒,
故答案为:7;
(2)已知0.01mol CH3COONa,则浓度为0.01mol•L-1的是Na+,HCl为0.002mol,则浓度为0.002mol•L-1的是Cl-,故答案为:Na+;Cl-;
(3)因反应前后的原子守恒,钠离子为0.01mol,则不符合两种微粒的物质的量之和等于0.01mol,由0.01molCH3COONa,根据醋酸根守恒可知,n(CH3COOH)+n(CH3COO-)=0.01mol,
故答案为:n(CH3COOH)+n(CH3COO-)=0.01mol.
点评 本题考查溶液中的微粒及电荷守恒、物料守恒,明确混合溶液中的溶质、电解质的强弱、原子守恒、电荷守恒是解答本题的关键,难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
10.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3.关于该物质的说法正确的是( )
| A. | 该物质属于盐类 | |
| B. | 该物质是Al(OH)3和Na2CO3的混合物 | |
| C. | 1mol NaAl(OH)2CO3最多可消耗3mol H+ | |
| D. | 该药剂不适合于胃溃疡患者服用 |
10.常温下,下列溶液中的粒子浓度关系正确的是( )
| A. | NH4Cl溶液中:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| B. | Na2SO4溶液中:c(Na+)+c(H+)=2c(SO42-)+c(OH-) | |
| C. | NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H+)>c(OH-) | |
| D. | 浓度均为0.1 mol/L的CH3COOH与CH3COONa溶液等体积混合所得溶液中:c (CH3COOH)+c(CH3COO-)=0.2mol/L |
14.25℃时有关弱酸的电离平衡常数关系为:Ki(CH3COOH)>Ki1(H2CO3)>Ki(HCN)>Ki2(H2CO3).在冰醋酸中逐滴加水,溶液导电性和加水体积的关系如图所示.下列说法正确的是( )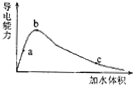

| A. | 等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) | |
| B. | 冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小 | |
| C. | 混合溶液中含有等物质的量的Na2CO3和NaHCO3,则一定存在c(Na+)+c(H+)═c(OH-)+c(HCO3-)+2c(CO32-) | |
| D. | a mol/LHCN溶液与b mol/LNaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则b一定大于a |
4.下列各组离子能在溶液中大量共存的是( )
| A. | HCO3-、Na+、OH-、K+ | B. | CO32-、Ba2+、K+、NO3- | ||
| C. | Ba2+、OH-、Cl-、Na+ | D. | CO32-、Na+、NO3-、H+ |
11.下列反应的离子方程式正确的是( )
| A. | 石英与烧碱溶液共热:SiO2+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$SiO32-+H2O | |
| B. | 在氯化铝溶液中滴加过量的氨水:Al3++4OH-=[Al(OH)4]- | |
| C. | 在氢氧化钠溶液中通入过量的CO2:2OH-+CO2=CO32-+H2O | |
| D. | 稀硫酸与氢氧化钡溶液反应H++SO42-+Ba2++OH-=BaSO4↓+H2O |
8.与0H?具有相同质子数和电子数的粒子是( )
| A. | F? | B. | C1? | C. | NH3 | D. | H2O |
9.分析下列各项结构的规律,按此规律排布第8项的分子式应为( )
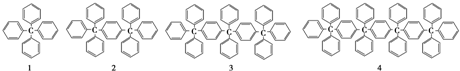

| A. | C158H118 | B. | C158H116 | C. | C160H116 | D. | C160H118 |

 .
.