题目内容
9.用纤维素为主要原料制备乙酸乙酯的路线如下: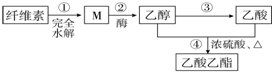
下列说法正确的是( )
| A. | ③和④都发生了氧化还原反应 | |
| B. | M虽然分子结构中无醛基,但仍然可以发生银镜反应 | |
| C. | 步骤②,1molM完全反应可以生成3mol乙醇 | |
| D. | 若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯 |
分析 由制备流程可知,纤维素水解生成M为葡萄糖,M在酒精酶的作用下分解生成乙醇,乙醇氧化生成乙酸,④中乙酸、乙醇发生酯化反应生成乙酸乙酯.
A.④为酯化反应,③为氧化反应;
B.M为葡萄糖,含-OH、-CHO;
C.步骤2发生C6H12O6→2C2H5OH+2CO2;
D.淀粉水解可生成葡萄糖.
解答 解:由制备流程可知,纤维素水解生成M为葡萄糖,M在酒精酶的作用下分解生成乙醇,乙醇氧化生成乙酸,④中乙酸、乙醇发生酯化反应生成乙酸乙酯.
A.只有③为氧化反应,故A错误;
B.M为葡萄糖,含-OH、-CHO,含-CHO可以发生银镜反应,故B错误;
C.步骤2发生C6H12O6→2C2H5OH+2CO2,1molM完全反应可以生成2mol乙醇,故C错误;
D.淀粉水解可生成葡萄糖,用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯,故D正确;
故选D.
点评 本题考查有机物的制备,为高频考点,把握有机物的性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物官能团与性质的关系,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
14.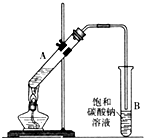 乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.有关数据及副反应:
乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.有关数据及副反应:
副反应:
C2H5OH+C2H5OH$→_{140℃}^{浓硫酸}$C2H5OC2H5+H2O
请回答下列问题:
(1)在大试管A中添加的试剂有6mL乙醇、4mL乙酸和4mL浓硫酸,这三种试剂的添加顺序依次为乙醇、浓硫酸、乙酸
(2)试管B中导管接近液面未伸入液面下的理由是防止发生倒吸
(3)现对试管B中乙酸乙酯粗产品进行提纯,步骤如下:
①将试管B中混合液体充分振荡后,转入分液漏斗(填仪器名称)进行分离;
②向分离出的上层液体中加入无水硫酸钠,充分振荡.加入无水硫酸钠的目的是:
③将经过上述处理的液体放入干燥的蒸馏烧瓶中,对其进行蒸馏,收集77.1℃左右的液体即得纯净的乙酸乙酯.
(4)从绿色化学的角度分析,使用浓硫酸制乙酸乙酯不足之处主要有产生大量的酸性废液污染环境,有副反应发生
(5)炒菜时,加一点白酒和醋能使菜肴昧香可口,试用符合实际情况的化学方程式解释:CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
 乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.有关数据及副反应:
乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.有关数据及副反应:| 乙酸 | 乙醇 | 乙酸乙酯 | C2H5OC2H5乙醚 | |
| 沸点/℃ | 118 | 78.3 | 77.1 | 34.5 |
| 溶解性 | 易溶于水 | 极易溶于水 | 与乙醚混溶 | 微溶于水 |
C2H5OH+C2H5OH$→_{140℃}^{浓硫酸}$C2H5OC2H5+H2O
请回答下列问题:
(1)在大试管A中添加的试剂有6mL乙醇、4mL乙酸和4mL浓硫酸,这三种试剂的添加顺序依次为乙醇、浓硫酸、乙酸
(2)试管B中导管接近液面未伸入液面下的理由是防止发生倒吸
(3)现对试管B中乙酸乙酯粗产品进行提纯,步骤如下:
①将试管B中混合液体充分振荡后,转入分液漏斗(填仪器名称)进行分离;
②向分离出的上层液体中加入无水硫酸钠,充分振荡.加入无水硫酸钠的目的是:
③将经过上述处理的液体放入干燥的蒸馏烧瓶中,对其进行蒸馏,收集77.1℃左右的液体即得纯净的乙酸乙酯.
(4)从绿色化学的角度分析,使用浓硫酸制乙酸乙酯不足之处主要有产生大量的酸性废液污染环境,有副反应发生
(5)炒菜时,加一点白酒和醋能使菜肴昧香可口,试用符合实际情况的化学方程式解释:CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
1.中学化学涉及多种常数,下列说法正确的是( )
| A. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| B. | 某温度下,2L密闭容器中加入4mol A和2mol B发生反应: 3A(g)+2B(g)?4C(s)+2D(g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=$\frac{{c}^{4}(C){c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$ | |
| C. | 温度一定时,当溶液中c(Ag+)•c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | |
| D. | 难溶电解质AB2饱和溶液中,c(A2+)=x mol•L-1,c(B-)=y mol•L-1,则Ksp值为4xy2 |
19.通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.现给出化学键的键能(见表):
请计算N2(g)+3H2(g)═2NH3(g)的反应热( )
| 化学键 | H-H | N三N | N-H |
| 键能/(kJ•mol-1) | 436 | 945.6 | 391 |
| A. | +192.4 kJ•mol-1 | B. | +92.4kJ•mol-1 | C. | -92.4kJ•mol-1 | D. | -192.4kJ•mol-1 |
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)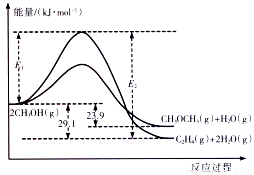
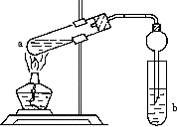 如图,在试管a中先加入2mL95%的乙醇,再加入3mL无水醋酸,边摇边缓缓加入2mL浓H2SO4,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
如图,在试管a中先加入2mL95%的乙醇,再加入3mL无水醋酸,边摇边缓缓加入2mL浓H2SO4,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
 .
.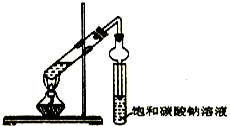 某同学用下列所示实验装置制取乙酸乙酯.回答以下问题:
某同学用下列所示实验装置制取乙酸乙酯.回答以下问题: