题目内容
16.化工厂中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱.(1)从物质的分类角度看,不恰当的一种物质是纯碱.
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时)H++OH-=H2O;2H++CO32-=CO2↑+H2O.
(3)“三酸”常用于溶解金属和金属氧化物.下列块状金属在常温时能全部溶于足量浓硝酸的是AB.
A.Ag B.Cu C.Al D.Fe
(4)烧碱、纯碱均可吸收CO2,当含0.1molNaOH的溶液吸收一定量CO2后,将溶液低温蒸干得到固体的组成可能有四种情况,分别是:①NaOH、Na2CO3;②Na2CO3;③Na2CO3、NaHCO3;④NaHCO3
(5)将(4)得到的固体重新溶解于水,在溶液中加盐酸,使溶液的PH=7,再将溶液蒸干,得到固体的质量是5.85g.
分析 (1)纯碱为Na2CO3,是由金属离子和酸根离子构成的;
(2)酸碱反应的实质是氢离子和氢氧根离子反应,而酸与碳酸盐的反应为氢离子与碳酸根离子反应;
(3)铁、铝在常温下遇浓硝酸发生钝化;
(4)根据CO2+2NaOH═Na2CO3+H2O、CO2+NaOH═NaHCO3来分析可能的组成;
(5)将得到的固体重新溶解于水,在溶液中加过量的盐酸,使其充分反应后,再将溶液蒸干,得到固体的质量为NaCl,利用Na原子守恒可计算NaCl的质量.
解答 解:(1)因碱电离产生的阴离子全部为OH-,而纯碱是由金属离子和酸根离子构成,则纯碱属于盐,而不属于碱,故答案为:纯碱;
(2)酸碱反应的实质是H++OH-=H2O,酸与可溶性碳酸盐的反应的实质为2H++CO32-=CO2↑+H2O,
故答案为:H++OH-=H2O;2H++CO32-=CO2↑+H2O;
(3)因浓硝酸具有强氧化性,则Ag、Cu在常温下能全部溶于浓硝酸,而Fe、Al遇浓硝酸发生钝化,而不能全部溶解,故答案为:AB;
(4)由CO2+2NaOH═Na2CO3+H2O、CO2+NaOH═NaHCO3可知,二氧化碳的物质的量小于0.1mol时溶质为NaOH、Na2CO3,等于0.1mol时溶质只有Na2CO3,0.1mol<n(CO2)<0.2mol时溶液的溶质为Na2CO3、NaHCO3,n(CO2)≥0.2mol时,溶液的溶质只有NaHCO3,故答案为:NaOH、Na2CO3;Na2CO3、NaHCO3;
(5)将得到的固体重新溶解于水,在溶液中加过量的盐酸,使其充分反应后,再将溶液蒸干,得到固体为NaCl,由Na原子守恒可知,n(NaCl)=n(NaOH)=0.1mol,其质量为0.1mol×58.5g/mol=5.85g,故答案为:5.85g.
点评 本题考查物质的分类,熟悉根据物质的组成和性质得出的分类结果、物质的性质是解答本题的关键,并学会利用化学反应及守恒法来进行计算,难度不大.

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案| A. | 5×10-13 mol•L-1 | B. | 0.02 mol•L-1 | ||
| C. | 1×10-7 mol•L-1 | D. | 1×10-12 mol•L-1 |
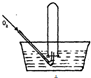 将体积为V mL的试管充满NO气体,按如图所示进行实验.当通入相同条件下O249mL时,液面仍在原来位置,则试管体积V为( )
将体积为V mL的试管充满NO气体,按如图所示进行实验.当通入相同条件下O249mL时,液面仍在原来位置,则试管体积V为( )| A. | 49mL | B. | 28 mL | C. | 30mL | D. | 24.5mL |
| A. | 8倍 | B. | 12倍 | C. | 24倍 | D. | 64倍 |
| A. | Na2CO3产生的CO2多 | B. | NaHCO3产生的CO2多 | ||
| C. | NaHCO3的反应速率快 | D. | 二者产生CO2一样多 |
| A. | 碳原子采取sp杂化 | B. | CO2晶胞是体心结构 | ||
| C. | 干冰是原子晶体 | D. | CO2为极性分子 |