题目内容
某探究小组利用丙酮的溴代反应(CH3COCH3+Br2
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v (Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:分析实验数据所得出的结论不正确的是( )
| HCl |
| 实验 序号 | 初始浓度 c/mol?L-1 | 溴颜色消失 所需时间 t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.8 | 0.2 | 0.001 | 290 |
| ② | 1.6 | 0.2 | 0.001 | 145 |
| ③ | 0.8 | 0.4 | 0.001 | 145 |
| ④ | 0.8 | 0.2 | 0.001 | 580 |
| A、v (Br2)与c(CH3COCH3)成正比 |
| B、增大c(Br2),v (Br2)变小 |
| C、增大c(HCl),v (Br2)增大 |
| D、实验②和③的v (Br2)相等 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:影响化学反应速率的因素有浓度、温度、压强以及催化剂等因素,一般情况下在其它条件相同时,反应物的浓度越大,反应速率越快,本题中溴作为反应物,其浓度越大,物质的量越多,其颜色消失的时间会越长,另外可从表中数据判断出,①④两组实验中CH3COCH3,HCl的浓度是相同的,而④中Br2比①中的大,所以时间变长,速率变慢.
解答:
解:A、对比①②组数据,可以判断出增大c(CH3COCH3),v(Br2)增大,故A正确;
B、对比①④两组实验中CH3COCH3,HCl的浓度是相同的,而④中Br2比①中的大,所以时间变长,但不能说明溴的反应速率大小问题,故C错误;
C、比较①③数据可以判断出,增大c(HCl),v(Br2)增大,故C正确;
D、比较实验②和③数据,Br2的浓度相等,溴颜色消失所需的时间也相等,溴的反应速率是相等的,故D正确;
故选B.
B、对比①④两组实验中CH3COCH3,HCl的浓度是相同的,而④中Br2比①中的大,所以时间变长,但不能说明溴的反应速率大小问题,故C错误;
C、比较①③数据可以判断出,增大c(HCl),v(Br2)增大,故C正确;
D、比较实验②和③数据,Br2的浓度相等,溴颜色消失所需的时间也相等,溴的反应速率是相等的,故D正确;
故选B.
点评:本题考查化学反应速率及其影响因素,做题时注意加强对表中数据的比较和分析,不难得出结论.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列各化合物的命名正确的是( )
| A、CH2=CH-CH=CH2 1,3-二丁烯 |
B、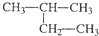 2-甲基丁烷 2-甲基丁烷 |
C、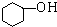 苯酚 苯酚 |
D、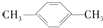 间二甲苯 间二甲苯 |
Na的化学性质很活泼,可以与水剧烈反应:2Na+2H2O=2NaOH+H2↑.该反应属于( )
| A、化合反应 | B、复分解反应 |
| C、置换反应 | D、分解反应 |
下列有关阿伏加德罗常数(NA)的说法正确的是( )
| A、32 g O2所含的原子数目为NA |
| B、1 mol氢约含有6.02×1023个微粒 |
| C、标准状况下,2NA 个H2O的体积约为44.8 L |
| D、标准状况下,22.4 L CH4和H2的混合气体中含有NA个分子 |
水的电离过程为H2O?H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是( )
| A、水的电离过程是吸热过程 |
| B、c(H+)随着温度的降低而升高 |
| C、在35℃时,纯水中c(H+)>c(OH-) |
| D、水的电离度α(25℃)>α(35℃) |