题目内容
磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质.已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解.
(1)已知:SO2 (g)+Cl2 (g)+SCl2 (g)?2SOCl2 (g)△H=a kJ?mol-1
SO2Cl2(g)+SCl2 (g)?2SOCl2(g)△H=b kJ?mol-1
则反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H= kJ?mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K= .
(2)磺酰氯可与白磷发生反应为:P4+10 SO2Cl2=4PCl5+10SO2↑,若生成1molSO2,则转移电子的物质的量为 mol.
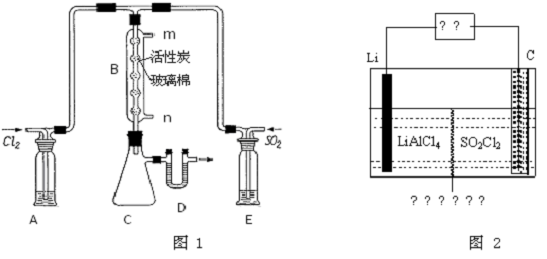
(3)某学习小组的同学依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计的制备磺酰氯装置如图1
①若用浓盐酸与二氧化锰为原料制取Cl2,其反应的化学方程式为 .
②有关题图1所示的装置说法正确的是 (不定项选择).
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为 .
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如题图2所示,已知电池反应为:2Li+SO2Cl2=2LiCl+SO2↑;则电池工作时,正极的电极反应式为 .
(1)已知:SO2 (g)+Cl2 (g)+SCl2 (g)?2SOCl2 (g)△H=a kJ?mol-1
SO2Cl2(g)+SCl2 (g)?2SOCl2(g)△H=b kJ?mol-1
则反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H=
(2)磺酰氯可与白磷发生反应为:P4+10 SO2Cl2=4PCl5+10SO2↑,若生成1molSO2,则转移电子的物质的量为
(3)某学习小组的同学依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计的制备磺酰氯装置如图1
①若用浓盐酸与二氧化锰为原料制取Cl2,其反应的化学方程式为
②有关题图1所示的装置说法正确的是
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如题图2所示,已知电池反应为:2Li+SO2Cl2=2LiCl+SO2↑;则电池工作时,正极的电极反应式为

考点:化学平衡常数的含义,热化学方程式,化学电源新型电池,制备实验方案的设计
专题:基本概念与基本理论,元素及其化合物
分析:(1)根据盖斯定律计算分析得到,和平衡常数表达式定义书写;
(2)由方程式可知P4+10 SO2Cl2=4PCl5+10SO2↑,P4~~10SO2~~20mole-,由此分析解答;
(3)①若用浓盐酸与二氧化锰为原料制取Cl2的方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
②a.A、E处洗气瓶,干燥吸水,二氧化硫和氯气都可以用浓硫酸干燥,而饱和食盐水和饱和NaHSO3溶液起不到干燥的作用,故错误;
b.B处反应管内五球中玻璃棉上的活性炭对氯气和二氧化硫的反应起催化作用,故正确;
c.B处反应管冷却水应低处进高处出,所以从n接口通入,故错误;
d.装置C处吸滤瓶应放在冰水中冷却,利平衡正向移动,提高产率,故正确;
e.D处U形管中盛放的固体干燥剂,可能是固体碱石灰,故正确;
③SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,正反应是放热反应,所以水冷却利于SO2Cl2的合成;
(4)正极是SO2Cl2中+6价的硫得电子发生还原反应.
(2)由方程式可知P4+10 SO2Cl2=4PCl5+10SO2↑,P4~~10SO2~~20mole-,由此分析解答;
(3)①若用浓盐酸与二氧化锰为原料制取Cl2的方程式为:MnO2+4HCl(浓)
| ||
②a.A、E处洗气瓶,干燥吸水,二氧化硫和氯气都可以用浓硫酸干燥,而饱和食盐水和饱和NaHSO3溶液起不到干燥的作用,故错误;
b.B处反应管内五球中玻璃棉上的活性炭对氯气和二氧化硫的反应起催化作用,故正确;
c.B处反应管冷却水应低处进高处出,所以从n接口通入,故错误;
d.装置C处吸滤瓶应放在冰水中冷却,利平衡正向移动,提高产率,故正确;
e.D处U形管中盛放的固体干燥剂,可能是固体碱石灰,故正确;
③SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,正反应是放热反应,所以水冷却利于SO2Cl2的合成;
(4)正极是SO2Cl2中+6价的硫得电子发生还原反应.
解答:
解:(1)SO2 (g)+Cl2 (g)+SCl2 (g)?2SOCl2 (g)△H=a kJ?mol-1…Ⅰ
SO2Cl2(g)+SCl2 (g)?2SOCl2(g)△H=b kJ?mol-1…Ⅱ
根据盖斯定律Ⅰ-Ⅱ得:SO2(g)+Cl2(g)?SO2Cl2(g)△H=(a-b )kJ?mol-1,平衡常数K=
,故答案为:(a-b );
;
(2)由方程式可知P4+10 SO2Cl2=4PCl5+10SO2↑,P4~~10SO2~~20mole-,所以生成1molSO2,则转移电子的物质的量为2mol,故答案为:2;
(3)①若用浓盐酸与二氧化锰为原料制取Cl2的方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
②a.A、E处洗气瓶,干燥吸水,二氧化硫和氯气都可以用浓硫酸干燥,而饱和食盐水和饱和NaHSO3溶液起不到干燥的作用,故错误;
b.B处反应管内五球中玻璃棉上的活性炭对氯气和二氧化硫的反应起催化作用,故正确;
c.B处反应管冷却水应低处进高处出,所以从n接口通入,故错误;
d.装置C处吸滤瓶应放在冰水中冷却,利平衡正向移动,提高产率,故正确;
e.D处U形管中盛放的固体干燥剂,可能是固体碱石灰,故正确;故选:bde;
③SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,正反应是放热反应,所以水冷却利于SO2Cl2的合成,故答案为:冷凝、降温均有利于SO2Cl2生成;
(4)正极是SO2Cl2中+6价的硫得电子发生还原反应,所以电极反应式为:SO2Cl2+2e-=2Cl-+SO2↑,故答案为:SO2Cl2+2e-=2Cl-+SO2↑.
SO2Cl2(g)+SCl2 (g)?2SOCl2(g)△H=b kJ?mol-1…Ⅱ
根据盖斯定律Ⅰ-Ⅱ得:SO2(g)+Cl2(g)?SO2Cl2(g)△H=(a-b )kJ?mol-1,平衡常数K=
| c(SO2Cl2) |
| c(SO2)?c(Cl2) |
| c(SO2Cl2) |
| c(SO2)?c(Cl2) |
(2)由方程式可知P4+10 SO2Cl2=4PCl5+10SO2↑,P4~~10SO2~~20mole-,所以生成1molSO2,则转移电子的物质的量为2mol,故答案为:2;
(3)①若用浓盐酸与二氧化锰为原料制取Cl2的方程式为:MnO2+4HCl(浓)
| ||
| ||
②a.A、E处洗气瓶,干燥吸水,二氧化硫和氯气都可以用浓硫酸干燥,而饱和食盐水和饱和NaHSO3溶液起不到干燥的作用,故错误;
b.B处反应管内五球中玻璃棉上的活性炭对氯气和二氧化硫的反应起催化作用,故正确;
c.B处反应管冷却水应低处进高处出,所以从n接口通入,故错误;
d.装置C处吸滤瓶应放在冰水中冷却,利平衡正向移动,提高产率,故正确;
e.D处U形管中盛放的固体干燥剂,可能是固体碱石灰,故正确;故选:bde;
③SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,正反应是放热反应,所以水冷却利于SO2Cl2的合成,故答案为:冷凝、降温均有利于SO2Cl2生成;
(4)正极是SO2Cl2中+6价的硫得电子发生还原反应,所以电极反应式为:SO2Cl2+2e-=2Cl-+SO2↑,故答案为:SO2Cl2+2e-=2Cl-+SO2↑.
点评:本题考查了盖斯定律和氧化还原的相关计算、化学方程式的书写、化学平衡常数的表达式、平衡移动和电极反应式的书写,难度不大,盖斯定律注意利用方程式相加减的方法处理.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
某探究小组利用丙酮的溴代反应(CH3COCH3+Br2
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v (Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:分析实验数据所得出的结论不正确的是( )
| HCl |
| 实验 序号 | 初始浓度 c/mol?L-1 | 溴颜色消失 所需时间 t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.8 | 0.2 | 0.001 | 290 |
| ② | 1.6 | 0.2 | 0.001 | 145 |
| ③ | 0.8 | 0.4 | 0.001 | 145 |
| ④ | 0.8 | 0.2 | 0.001 | 580 |
| A、v (Br2)与c(CH3COCH3)成正比 |
| B、增大c(Br2),v (Br2)变小 |
| C、增大c(HCl),v (Br2)增大 |
| D、实验②和③的v (Br2)相等 |
下列化学用语正确的是( )
| A、氟化氢的电子式:H:F |
| B、乙醇的分子式:CH3CH2OH |
C、硫原子的结构示意图: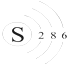 |
| D、Na2O2中即含有离子键,又含有非极性共价键 |
想一想:NaOH、CuSO4、CH3COOH这些物质为什么可以归为一类,下列哪些物质还可以和它们归为一类( )
| A、CO2 |
| B、HCl(气态) |
| C、Fe(OH)3胶体 |
| D、NaOH溶液 |
下列变化属于化学变化的是( )
| A、从CuSO4溶液中提取单质铜 |
| B、浓盐酸的挥发 |
| C、从浓食盐水中得到氯化钠晶体 |
| D、用CCl4萃取溴水中的溴 |