题目内容
8.同温同压下,相同体积的CO和C2H4的比较中正确的是( )①所含的分子数目之比为1:1 ②所含的质子数目之比为1:1
③所含的原子总数目之比为1:3 ④两者的密度之比为:1:1.
| A. | ①②③④ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
分析 同温同压下,气体摩尔体积相同,则相同体积的CO和C2H4具有相同的物质的量,
①物质的量相同时,含有的分子数一定相同;
②CO分子含有14个质子,C2H4分子含有16个质子,物质的量相同时含有的质子数不同;
③CO分子含有2个原子,C2H4含有6个原子,结合二者物质的量计算含有原子数之比;
④二者的摩尔质量都是28g/mol,根据ρ=$\frac{M}{{V}_{m}}$判断.
解答 解:同温同压下,气体摩尔体积相同,则相同体积的CO和C2H4具有相同的物质的量,
①根据n=nNA可知,二者所含的分子数相等,其分子数目之比为1:1,故①正确;
②所含的质子数目之比=质子物质的量之比=(1×14):(1×16)=7:8,故②错误;
③CO和C2H4分子分别含有原子数为2、6,物质的量相等时含有的原子数之比=原子的物质的量之比=(1×2):(1×6)=1:3,故③正确;
④二者摩尔质量相等,ρ=$\frac{M}{{V}_{m}}$可知两者的密度相等,其密度之比=1:1,故④正确;
故选D.
点评 本题考查了阿伏伽德罗定律及推论的应用,题目难度中等,明确阿伏伽德罗定律内容为解答关键,注意掌握物质的量与其它物理量之间的转化关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
18.下列关于有机化合物的说法正确的是( )
| A. | 以淀粉为原料可制取乙酸乙酯 | B. | 聚氯乙烯分子中含碳碳双键 | ||
| C. | 丁烷有3种同分异构体 | D. | 油脂的皂化反应属于加成反应 |
19.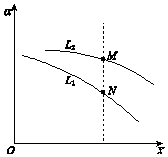 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )| A. | X表示温度 | B. | L2>L1 | C. | 反应速率 υ(M)>υ(N) | D. | 平衡常数 K(M)>K(N) |
16.化学反应中,反应物用量、浓度或反应条件不同可能对生成物产生影响.下列反应的生成物不受上述因素影响的是( )
| A. | 铜与硝酸反应 | B. | 钠与氧气反应 | ||
| C. | 氢气与氯气反应 | D. | 氯化铝与氢氧化钠溶液反应 |
3.下列关于安全事故的处理方法中,正确的是( )
| A. | 皮肤上不慎沾上浓Na OH溶液,立即用稀硫酸冲洗 | |
| B. | 大量氯气泄漏时,应迅速离开现场,并尽快往高处去 | |
| C. | 不慎洒出的酒精在桌上着火时,立即用大量水扑灭 | |
| D. | 金属钠着火时,应立即用沾水的毛巾覆盖 |
13.乙烷混有乙烯,欲除去乙烯得到纯净干燥的乙烷,下列方法正确的( )
| A. | 依次通过溴水、烧碱、浓硫酸 | B. | 依次通过酸性KMnO4溶液、浓硫酸 | ||
| C. | 依次通过澄清石灰水、浓硫酸 | D. | 通入氢气,在一定条件下反应 |
20.在多电子原子中,决定轨道能量的是( )
| A. | 电子层 | B. | 电子层和能级 | ||
| C. | 电子层、能级和原子轨道空间分布 | D. | 原子轨道空间分布和电子自旋方向 |
17.下列物质的水溶液因水解而呈酸性的是( )
| A. | CuCl2 | B. | Na2CO3 | C. | CH3COOH | D. | KHSO4 |
18.下列化学用语的表达正确的是( )
| A. | 硫酸的电离方程式:H2SO4=H2++SO42- | |
| B. | 光导纤维主要成分的化学式:Si | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| D. | 钠离子的结构示意图: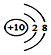 |