题目内容
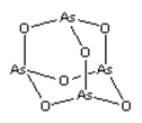
【题目】As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl3,AsCl3用LiAlH4还原生成AlH3。下列说法正确的是( )
A.As2O3分子中As原子的杂化方式为sp2
B.LiAlH4为共价化合物,含有配位键
C.AsCl3空间构型为平面正三角形
D.AlH3分子键角大于109.5°
【答案】D
【解析】
A.As2O3中As原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断As原子杂化类型为sp3,A错误;
B.只含共价键的化合物为共价化合物,含有离子键的化合物为离子化合物,该物质是由Li+和AlH4-构成的,为离子化合物,B错误;
C.AsCl3中As原子价层电子对个数为4且含有一个孤电子对,根据价层电子对互斥理论判断其空间构型为三角锥形,C错误;
D.AlH3中Al原子价层电子对个数为3且不含孤电子对,根据价层电子对互斥理论,为平面正三角形,所以其键角为120°,大于109.5°,D正确;
故选D。

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
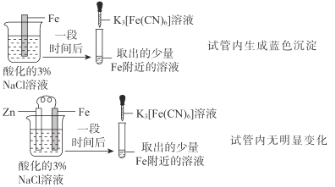
A |
| Zn保护了Fe不被腐蚀 |
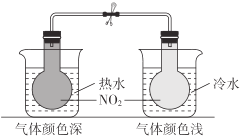
B |
| 2NO2(g)N2O4(g)为吸热反应 |
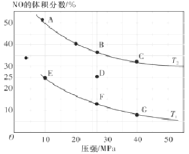
C |
| 木炭与浓硝酸发生了反应 |
D |
| 碳酸钠的水解程度强 |
A.AB.BC.CD.D