题目内容
5.下列有关说法错误的是( )①NaHCO3溶液加水稀释,$\frac{c(N{a}^{+})}{c(HC{O}_{3}^{-})}$的值保持增大
②浓度均为0.1mol/L的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1mol/L氨水中滴加0.1mol/L盐酸,恰好完全反应时溶液的pH=6,则由水电离产生的c(H+)=10-6mol/L
④在Na2S稀溶液中,c(OH-)=c(H+)+c(H2S)+c(HS-)
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
分析 ①稀释,促进电离,钠离子物质的量不变,碳酸氢根离子的物质的量减小;
②浓度均为0.1mol/L的Na2CO3、NaHCO3混合溶液,2n(Na)=3n(C);
③恰好完全反应时溶液的pH=6,反应生成氯化铵,水解显酸性;
④溶液中遵循质子守恒.
解答 解:①NaHCO3溶液加水稀释,促进HCO3-的水解,n(HCO3-)减小,n(Na+)不变,则$\frac{c(N{a}^{+})}{c(HC{O}_{3}^{-})}$的比值会增大,故①正确;
②浓度均为0.1mol•L-1的Na2CO3、NaHCO3混合溶液,假设体积为1L,则n(Na+)=0.3mol,而c(CO32-)+c(HCO3-)+c(H2CO3)=0.2mol,则:2c(Na+)=3[c(CO32-)+c(H2CO3)+c(HCO3-)],故②错误;
③在0.1mol•L-1氨水中滴加0.1mol•L-1盐酸,刚好完全中和生成氯化铵,铵根离子水解促进了水的电离,此时pH=6,则溶液中水电离的c(OH-)=c(H+)=10-6mol•L-1,故③正确;
④在Na2S稀溶液中,根据质子守恒可得:c(OH-)=c(H+)+2c(H2S)+c(HS),故④错误;
故选D.
点评 本题考查弱电解质的电离平衡,为高频考点,把握盐类水解、酸碱混合及pH的计算等为解答的关键,侧重分析与应用能力的考查,注意质子守恒及原子守恒的应用,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
15.下列关于有机物的说法正确的是( )
| A. | 有机物不能通过人工的方法合成 | |
| B. | 烃是指燃烧后只生成CO2和H2O的有机物 | |
| C. | 有机物只含有碳、氢两种元素 | |
| D. | 含碳元素的化合物不一定都属于有机物 |
20.X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示,已知X、Y、Z的质子数之和为31.试回答:
(1)它们的元素符号是C;Mg;Al.
(2)X的最高价氧化物的化学式为CO2,X元素的最简单气态氢化物的分子式为CH4.
(3)Z的最高价氧化物是两性(选填“两性”“酸性”或“碱性”)氧化物.
(4)Y与水反应的化学方程式2Mg+2H2O═Mg(OH)2+H2↑.
| X | ||
| Y | Z |
(2)X的最高价氧化物的化学式为CO2,X元素的最简单气态氢化物的分子式为CH4.
(3)Z的最高价氧化物是两性(选填“两性”“酸性”或“碱性”)氧化物.
(4)Y与水反应的化学方程式2Mg+2H2O═Mg(OH)2+H2↑.
10. 实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O.
(2)装置B的作用是平衡压强,作安全瓶,防止倒吸.
(3)在装置C中应加入c(填字母).
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)若产物中有少量未反应的Br2,最好用e(填字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是产品熔点低,过度冷却会凝固而堵塞导管口.
(7)判断该制备反应已经结束的最简单方法是D中溴水完全褪色.
 实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:| 乙醇 | 1,2-二溴乙烷 | 醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)烧瓶A中发生的主要的反应方程式CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O.
(2)装置B的作用是平衡压强,作安全瓶,防止倒吸.
(3)在装置C中应加入c(填字母).
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)若产物中有少量未反应的Br2,最好用e(填字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是产品熔点低,过度冷却会凝固而堵塞导管口.
(7)判断该制备反应已经结束的最简单方法是D中溴水完全褪色.
17.X、Y、Z、W、R属于短周期主族元素.X的原子半径是短周期主族元素中最大的,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1. 下列叙述错误的是( )
| A. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y的氢化物比R的氢化物稳定,熔沸点高 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z | |
| D. | RY2、WY2通入Ba(NO3)2溶液中均无白色沉淀生成 |
4.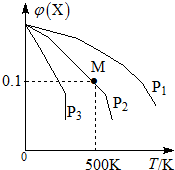 某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )
某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )
 某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )
某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )| A. | 升高温度,该反应平衡常数K减小 | |
| B. | 压强大小有P3>P2>P1 | |
| C. | 平衡后加入高效催化剂使气体相对分子质量增大 | |
| D. | 在该条件下M点X平衡转化率为$\frac{9}{11}$ |
 、
、 ;
;