题目内容
4.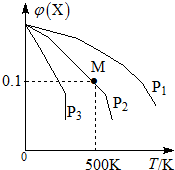 某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )
某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )| A. | 升高温度,该反应平衡常数K减小 | |
| B. | 压强大小有P3>P2>P1 | |
| C. | 平衡后加入高效催化剂使气体相对分子质量增大 | |
| D. | 在该条件下M点X平衡转化率为$\frac{9}{11}$ |
分析 可逆反应2X(g)?3Y(g)+Z(g)为气体体积增大的反应,则增大压强平衡逆向移动,X的物质的量分数增大,由图象可知升高温度,X的含量减小,则平衡正向移动,说明正反应为吸热反应,平衡常数增大,反应从X开始,M点对应的平衡体系中,X的体积分数为0.1,可设起始量为1mol,转化xmol,结合三段法列式计算,以此解答该题.
解答 解:A.根据图象知,升高温度,X转化率降低,说明反应向正方向移动,平衡常数增大,故A错误;
B.可逆反应的正反应是气体分子数增大的反应,减小压强,X转化率增大,所以,压强大小关系有:P3<P2<P1,故B错误;
C.催化剂不会使平衡发生移动,气体相对分子质量不变,故C错误;
D.M点对应的平衡体系中,X的体积分数为0.1.用三段法计算:
2X(g) 3Y(g)+Z(g)
3Y(g)+Z(g)
起始:1 0 0
变量:2x 3x x
平衡:1-2x 3x x
$\frac{1-2x}{1+2x}$=0.1,x=$\frac{9}{22}$,X转化率为$\frac{2x}{1}$=$\frac{2×9}{22}$=$\frac{9}{11}$.故D正确.
故选D.
点评 本题旨在考查学生对化学平衡图象的理解,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握图象曲线变化的特点,结合方程式的特征以及平衡移动的影响因素解答该类题目,难度中等.

练习册系列答案
相关题目
6.某炔烃与氢气加成后得到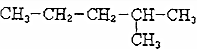 ,该炔烃可能有的结构式有( )
,该炔烃可能有的结构式有( )
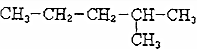 ,该炔烃可能有的结构式有( )
,该炔烃可能有的结构式有( )| A. | 一种 | B. | 二种 | C. | 三种 | D. | 四种 |
19.天津港“8•12”危化仓库爆炸,造成生命、财产重大损失,其爆炸品中有金属钠.运输金属钠的集装箱应贴有的警示标识是( )
| A. |  氧化剂 | B. |  爆炸品 | C. |  剧毒品 | D. |  遇湿易燃物品 |
16.下列关于平衡移动的说法不正确的是( )
| A. | 当正反应与逆反应速率相等时,平衡不移动 | |
| B. | 当正反应大于逆反应速率时,平衡向正反应方向移动 | |
| C. | 当正反应小于逆反应速率时,平衡向正反应方向移动 | |
| D. | 反应速率发生改变,平衡不一定发生移动 |
13.下列有机物命名正确的是( )
| A. |  二乙酸乙二酯 二乙酸乙二酯 | B. |  2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | C. |  2-甲基-1-丙醇 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |
14.常温下将铁放入下列过量的溶液中,在溶液中能大量生成Fe3+的是( )
| A. | 浓硫酸 | B. | 浓硝酸 | C. | 稀硝酸 | D. | 盐酸 |