题目内容
4.下列与标准状况下6.72L SO2气体含有氧原子数相同的是( )| A. | 标准状况下6.72 L CO | B. | 0.3NA个Na2SO3 | ||
| C. | 常温常压下9.6g O2 | D. | 1.806×1023个H2O分子 |
分析 n(SO2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,含有O原子为0.6mol,根据n=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$计算选项中各物质的物质的量,再结合化学式计算氧原子物质的量,据此判断.
解答 解:n(SO2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,含有O原子为0.3mol×2=0.6mol,
A.标准状况下6.72 L CO的物质的量为,n(SO2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,则n(O)=n(CO)=0.3mol,故A不符合;
B.0.3NA个Na2SO3的物质的量为0.3mol,含有O原子为0.3mol×3=0.9mol,故B不符合;
C.常温常压下9.6g O2的物质的量为$\frac{9.6g}{32g/mol}$=0.3mol,含有O原子为0.3mol×2=0.6mol,故C符合;
D.1.806×1023个H2O分子物质的量为$\frac{1.806×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.3mol,含有O原子为0.3mol×1=0.3mol,故D不符合,
故选C.
点评 本题考查物质的量有关计算,注意对化学式的理解,侧重对学生基础知识的巩固.

练习册系列答案
相关题目
15.法国化学家伊夫•肖万获2005年诺贝尔化学奖.他发现了烯烃里的碳-碳双键会被拆散、重组,形成新分子,这种过程被命名为烯烃复分解反应.烯烃复分解反应可形象地描述为交换舞伴.(如图所示)

烯烃复分解反应中的催化剂是金属卡宾(如CH2=M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈.随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴.后者会继续寻找下一个烯烃分子,再次“交换舞伴”.把C6H5CH2CH=CH2与CH2=M在一定条件下混合反应,下列产物不可能存在的是( )

烯烃复分解反应中的催化剂是金属卡宾(如CH2=M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈.随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴.后者会继续寻找下一个烯烃分子,再次“交换舞伴”.把C6H5CH2CH=CH2与CH2=M在一定条件下混合反应,下列产物不可能存在的是( )
| A. | C6H5CH2CH=M | B. | CH2=CH2 | ||
| C. | C6H5CH2CH2C6H5 | D. | C6H5CH2CH=CHCH2C6H5 |
12.某矿石样品中可能含铁,为确定其成分,进行如下操作:

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 向溶液乙中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在Fe3+ | |
| B. | 向溶液乙中滴加少量氢氧化钠溶液,一定出现红褐色沉淀 | |
| C. | 向溶液甲中滴加KSCN溶液,溶液颜色变红,则原矿石样品中存在Fe3+ | |
| D. | 该矿石一定为赤铁矿 |
19.一定温度下可逆反应N2(g)+3H2(g)?2NH3(g)达平衡的标准是:(分别用V(正)表示正反应速率,V(逆)表示逆反应速率)( )
| A. | 2V(正)(N2)=V(逆)(NH3) | B. | V(正)(N2)=3V(正)(H2) | ||
| C. | 2V(正)(H2)=3V(逆)(NH3) | D. | N2、H2、NH3的体积比为1:3:2 |
16.工业上制取金刚砂的化学反应方程式如下:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为( )
| A. | 1:2 | B. | 2:1 | C. | 1:3 | D. | 3:1 |
13.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( )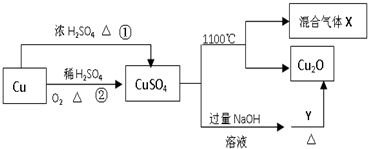

| A. | 途径①和途径②都体现了硫酸的酸性和氧化性 | |
| B. | 将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体 | |
| C. | CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 | |
| D. | Y可以是酒精溶液 |
14.2.3g纯净物金属钠在干燥空气中被氧化后得到3.5g固体,由此可判断其氧化产物是( )
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O和Na2O2 | D. | 无法确定 |

 ,比较S2-与Cl-的半径大小:r(S2-)>(填“>”或“<”)r(Cl-).
,比较S2-与Cl-的半径大小:r(S2-)>(填“>”或“<”)r(Cl-).