题目内容
16.工业上制取金刚砂的化学反应方程式如下:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为( )| A. | 1:2 | B. | 2:1 | C. | 1:3 | D. | 3:1 |
分析 SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑中,C元素的化合价由0升高为+2价,C元素的化合价由0降低为-4价,以此来解答.
解答 解:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑中,C元素的化合价由0升高为+2价,C元素的化合价由0降低为-4价,
则C为氧化剂,也是还原剂,
由电子守恒及原子守恒可知,1molC作氧化剂与2molC作还原剂转移电子相等,
则氧化剂和还原剂物质的量之比为1:2,
故选A.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
6.下列叙述中正确的是( )
| A. | 氧化钠溶于水与水反应后电离生成钠离子和氢氧根离子,因而氧化钠是非电解质 | |
| B. | NH3、SO3的水溶液均导电,所以NH3、SO3均是电解质 | |
| C. | 能电离出H+的化合物都是酸,能电离出OH-的化合物都是碱 | |
| D. | 液态HCl、固体NaCl均是电解质,但液态HCl和固体NaCl均不导电 |
4.下列与标准状况下6.72L SO2气体含有氧原子数相同的是( )
| A. | 标准状况下6.72 L CO | B. | 0.3NA个Na2SO3 | ||
| C. | 常温常压下9.6g O2 | D. | 1.806×1023个H2O分子 |
1.下列说法中,正确的是( )
| A. | 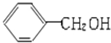 与 与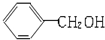 互为同系物 互为同系物 | B. | 乙醇和二甲醚互为同分异构体 | ||
| C. | 乙醇、乙二醇、丙三醇互为同系物 | D. | 可用浓溴水来区分乙醇和苯酚 |
8.下列各组物质中,依次属于单质、酸、盐的一组是( )
| A. | 干冰、石灰石、氧化钙 | B. | 液氯、硝酸、纯碱 | ||
| C. | 水、烧碱、食盐 | D. | 氧气、盐酸、熟石灰 |
5.NA代表阿伏加德罗常数的数值,下列有关NA的叙述中,正确的是( )
| A. | 1mol任何物质所含的分子数均为NA个 | |
| B. | 14 g氮气所含的N原子数为NA个 | |
| C. | 标准状况下,22.4 L SO3中所含分子数为NA个 | |
| D. | 在钠与氯气的反应中,1 mol氯气失去电子的数目为2NA个 |