题目内容
如下反应:2A(g)+3B(g)?2C(g)+D(g),在四种不同条件下的反应速率分别为:①V(A)=0.5mol?L-1?s-1②V(B)=0.6mol?L-1?s-1③V(C)=0.3mol?L-1?s-1④V(D)=0.4mol?L-1?s-1则该反应在四种不同条件下反应速率最快的是( )
| A、① | B、② | C、③ | D、④ |
考点:化学反应速率和化学计量数的关系
专题:化学反应速率专题
分析:化学反应速率之比等于化学计量数之比,则反应速率与化学计量数的比值越大,则反应速率越大,以此来解答.
解答:
解:①V(A)=0.5mol?L-1?s-1,则
=0.25;
②V(B)=0.6mol?L-1?s-1,则
=0.2;
③V(C)=0.3mol?L-1?s-1,则
=0.15;
④V(D)=0.4mol?L-1?s-1,则
=0.4,
则D表示的反应速率最快,
故选D.
| 0.5 |
| 2 |
②V(B)=0.6mol?L-1?s-1,则
| 0.6 |
| 3 |
③V(C)=0.3mol?L-1?s-1,则
| 0.3 |
| 2 |
④V(D)=0.4mol?L-1?s-1,则
| 0.4 |
| 1 |
则D表示的反应速率最快,
故选D.
点评:本题考查反应速率的比较,为高频考点,把握化学计量数与反应速率的关系为解答的关键,注意利用比值法可快速比较,也可转化为同种物质的反应速率比较,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些酸和醇重新组合可形成的酯共有( )
| A、28种 | B、32种 |
| C、40种 | D、48种 |
四种短周期元素W、X、Y、Z,其原子的最外层电子数之和为19,W和X元素原子的质子数之比为1:2,Y的核外电子数比X多4,X2+和Z-离子的电子数之差为8.下列说法中,正确的是( )
| A、原子半径大小:Z>Y>X>W |
| B、Y、Z两种元素的氧化物对应的水化物酸性为:Y<Z |
| C、X、Y、Z三种元素的单质均既有氧化性又有还原性 |
| D、W、Y、Z三种元素形成的气态氢化物中最稳定的是Z的气态氢化物 |
如图为元素周期表短周期的一部分.下列关于A~F六种元素的叙述正确的是( )

| A、A、B、D、E四种元素所形成的最高价含氧酸中D的酸性最强 |
| B、形成的简单阴离子半径的大小顺序为:C>B>D>E |
| C、D、E、F三种元素形成的单质中都含有共价键 |
| D、1 mo1A、B、C元素的简单氢化物中都含有10 mol电子 |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、1Llmol/L的Na2CO3溶液中含有的CO32-数目为NA |
| B、1mol羟基(-OH)所含的电子数约为l0NA |
| C、1mol丙烯分子有2molσ键,1molπ键 |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
自然界中存在一种尖晶石,化学式为MgAl2O4,它透明色美,可作宝石.已知该尖晶石中混有Fe2O3.5.68g该样品恰好能完全溶解在100mL一定浓度的盐酸中,则该盐酸的浓度可能是( )
| A、4.6mol/L |
| B、3.2mol/L |
| C、2.5mol/L |
| D、1.2mol/L |
把95g含有某一种氯化物杂质的氯化镁粉末溶于水后,与足量AgNO3溶液反应,生成300g AgCl沉淀,则该氯化镁中的杂质可能是( )
| A、NaCl |
| B、A1C13 |
| C、KCl |
| D、CaCl2 |
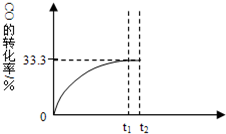 某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应:
某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应: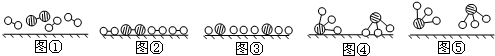
 、
、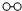 、
、 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面.分别写出图②→③、图③→④表示的变化过程
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面.分别写出图②→③、图③→④表示的变化过程