题目内容
5.下列分子中所有原子都满足最外层8电子结构的是( )| A. | NH3 | B. | PCl5 | C. | CO2 | D. | CO(NH2)2 |
分析 对于共价化合物,元素化合价的绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,据此进行判断.
解答 解:A.NH3中,N原子的最外层电子为:5+|-3|=8,H原子的最外层电子为:1+1=2,不都满足8电子稳定结构,故A错误;
B.PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故B错误;
C.CO2中C元素化合价为+4,C原子最外层电子数为4,所以4+4=8,分子中C原子满足8电子结构;O元素化合价为-2,O原子最外层电子数为6,所以|-2|+6=8,分子中O原子满足8电子结构,故C正确;
D.CO(NH2)2中,H原子的最外层电子为:1+1=2,不满足8电子稳定结构,故D错误;
故选C.
点评 本题考查分子8电子结构判断,题目难度不大,本题是对共价键的理解,掌握判断规律|化合价|+元素原子的最外层电子数=8,满足最外层8电子结构,注意分子有H原子一定不满足8电子结构.

练习册系列答案
相关题目
16.在较高温度下的某溶液中,硝酸钾、氯化钠均达饱和,冷却析出晶体的成分是( )
| A. | 纯硝酸钾晶体 | B. | 大量硝酸钾晶体,少量氯化钠 | ||
| C. | 等量的硝酸钾和氯化钠 | D. | 大量氯化钠,少量硝酸钾 |
20.下列叙述正确的是( )
| A. | 同周期元素的原子半径以ⅦA族的为最大 | |
| B. | 短周期中次外层电子数是最外层电子数2倍的原子一定是非金属元素 | |
| C. | 同主族两种元素原子的核外电子数的差值可能为26 | |
| D. | 科学家在周期表中金属元素与非金属元素分界线处找到了优良的催化剂 |
10.如图是从元素周期表中截取下来的,A,B,C为短周期主族元素,下列说法中正确的是( )
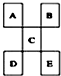

| A. | D一定是金属元素,其金属性比C强 | |
| B. | C的最高价氧化物水化物显强酸性 | |
| C. | B的氢化物是以分子形式存在,且某些分子间存在氢键 | |
| D. | E的原子序数一定是A的5倍,且原子半径比A大 |
17.下列说法不正确的是( )
| A. | 使用催化剂,可以加快反应速率 | |
| B. | 可逆反应A(g)?B(g)+C(g),增大压强正反应速率和逆反应速率增大 | |
| C. | 对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大 | |
| D. | 参加反应物质的性质是决定化学反应速率的主要因素 |
14.对复杂的有机物结构可用“键线式”表示.如苯丙烯酸1-丙烯酯: 可简化为
可简化为 杀虫剂“阿乐丹”的结构表示为
杀虫剂“阿乐丹”的结构表示为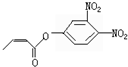 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
 可简化为
可简化为 杀虫剂“阿乐丹”的结构表示为
杀虫剂“阿乐丹”的结构表示为 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )| A. | 均能发生银镜反应 | B. | 遇FeCl3溶液均显紫色 | ||
| C. | 均能与NaHCO3溶液发生反应 | D. | 均能与浓溴水发生反应 |
15.某元素R的核外电子数等于核内中子数,取该元素的单质5.60g与氧气充分反应,可以得到12.0g化合物RO2,则元素R在元素周期表中的位置是( )
| A. | 第二周期 IVA族 | B. | 第三周期 IV A族 | C. | 第三周期 VI A族 | D. | 第二周期VI A族 |